题目内容
4.如图所示为甲、乙两种固体的溶解度曲线,下列说法错误的是( )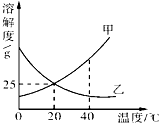
| A. | 甲、乙两种物质的溶解度都随温度的升高而增大 | |
| B. | 若甲固体中含有少量乙,可采用降温结晶的方法提纯甲 | |
| C. | 20℃时,把30 g甲物质加入100 g水中,充分溶解后所得溶液为饱和溶液 | |
| D. | 40℃时,甲的溶解度大于乙的溶解度 |
分析 A、据溶解度曲线可知物质的溶解度随温度变化情况;
B、甲的溶解度随温度升高而增大,乙的溶解度随温度升高而减小,所以若甲固体中含有少量乙,可用降温结晶的方法提纯甲;
C、据该温度下甲的溶解度分析解答;
D、据溶解度曲线可比较同一温度下不同物质的溶解度大小.
解答 解:A、乙的溶解度随温度的升高而减小,故错误;
B、甲的溶解度随温度升高而增大,乙的溶解度随温度升高而减小,所以若甲固体中含有少量乙,可用降温结晶的方法提纯甲,正确;
C、20℃时甲的溶解度是25g,即100g水中最多溶解25g的甲,所以把30 g甲物质加入100 g水中,充分溶解后剩余5g溶质,所得溶液为饱和溶液,正确;
D、由溶解度曲线可知:40℃时,甲的溶解度大于乙的溶解度,正确;
故选:A.
点评 明确溶解度概念的含义、溶解度曲线的意义即可顺利解答,属于基础知识考查题.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.以下符号既能表示一种元素又能表示一个原子还能表示某种物质的是( )
| A. | Fe | B. | N | C. | O2 | D. | Cl |
12.2008年是奥运年,历届奥运会形式都要进行圣火点燃仪式.2008年北京奥运火炬的燃料是丙烷(C3H8),它燃烧时火苗高且明亮.下列关于丙烷的叙述不正确的是( )
| A. | 丙烷是由C、H两种元素组成的 | B. | 丙烷燃烧产物是CO2和H2O | ||
| C. | 丙烷由3个C原子和8个H原子组成 | D. | 丙烷的相对分子质量是44 |
19.将一瓶盐酸分成三等份,并分别放入三个烧杯中,再在三个烧杯中分别加入等质量的镁、锌、铁三种金属.等反应结束后,三种金属均有剩余,且剩余金属质量为m(镁)>m(铁)>m(锌).若镁、铁、锌生成氢气的质量分别用a、b、c表示,则a、b、c三者的大小关系是( )
| A. | a<b<c | B. | a=b>c | C. | a>b=c | D. | a=b=c |
9.小彬同学家新买了水龙头,他从说明书上了解到该水龙头是铜质镀铬的.想起在学习金属性质时用到的金属活动性顺序中没有铬,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,小彬进行了如下探究的活动.
【查阅资料】铬(Cr)是银白色、有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液…
铝是银白色、有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【猜想与预测】三种金属在金属活动性顺序中的相对位置关系:①Cr、Al、Cu;②Al、Cr、Cu;③Al、Cu、Cr.
【实验验证】取大小相同的三种金属薄片,用砂纸打磨光亮(除去金属表面的氧化物)
【反思交流】
(1)请将上述实验现象或结论填写完整.
(2)实验一发生反应的化学方程式是:Cr+H2SO4═CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是无法比较铬和铝的金属活动性强弱.
【归纳提升】
(1)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,如:Al、CrSO4溶液、Cu这三种药品.
(2)比较金属活动性强弱的方法有:
①通过金属与酸反应,判断金属活动性强弱②通过金属与盐溶液反应,判断金属活动性强弱.
【查阅资料】铬(Cr)是银白色、有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜.铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液…
铝是银白色、有光泽的金属,能与稀硫酸反应,生成无色的硫酸铝溶液…
【猜想与预测】三种金属在金属活动性顺序中的相对位置关系:①Cr、Al、Cu;②Al、Cr、Cu;③Al、Cu、Cr.
【实验验证】取大小相同的三种金属薄片,用砂纸打磨光亮(除去金属表面的氧化物)
| 实验一 | 实验二 | 实验三 | |
| 实验方案 | 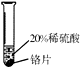 | 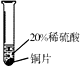 | 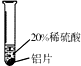 |
| 实验现象 | 铬片表面产生气泡缓慢,溶液变蓝色 | 无现象 | 铝片表面产生气泡较快 |
| 结论 | 铬能与稀硫酸发生反应,反应速率较慢 | 铜不与稀硫酸反应 | 铝能与稀硫酸发生反应,反应速率较快 |
| 三种金属在金属活动性顺序中的相对位置关系是②(填序号) | |||
(1)请将上述实验现象或结论填写完整.
(2)实验一发生反应的化学方程式是:Cr+H2SO4═CrSO4+H2↑.
(3)小东提出用硫酸铜溶液代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是无法比较铬和铝的金属活动性强弱.
【归纳提升】
(1)小清认为只要选用三种药品进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,如:Al、CrSO4溶液、Cu这三种药品.
(2)比较金属活动性强弱的方法有:
①通过金属与酸反应,判断金属活动性强弱②通过金属与盐溶液反应,判断金属活动性强弱.
14.对大气都有严重污染的一组有害气体是( )
| A. | 一氧化碳 二气化碳 氧气 | B. | 二氧化碳 甲烷 二氧化硫 | ||
| C. | 一氧化碳 二氧化氮 二氧化硫 | D. | 氢气 一氧化碳 硫化氢 |
 目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要.
目前,我们国家的能源主要依赖于化石燃料,它们属于不可再生资源.因此,开发利用新能源就显得格外重要.