题目内容
19.某学习小组用下列装置进行CO2的制取及性质探究实验.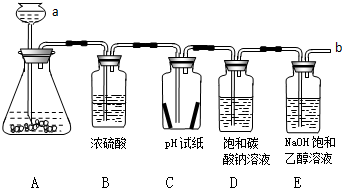
资料卡片:20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g.
请根据上图回答下列问题:
(1)图中装置A是用大理石制CO2的装置,仪器a的名称是长颈漏斗;装置A中发生反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑;在b处检验是否有CO2逸出的操作是将燃着的木条放在导气管口,观察木条是否熄灭.
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,实验结论是CO2与水反应后的溶液显酸性.
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,则反应的化学方程式是Na2CO3+CO2+H2O=2NaHCO3↓.
(4)当通入CO2一段时间后,装置E中观察到的实验现象是出现白色沉淀(或浑浊),则发生反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
分析 (1)根据常见的化学仪器的名称,根据实验室中制取二氧化碳的反应原理、二氧化碳的检验方法,进行分析解答.
(2)根据湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,说明有酸性物质生成,进行分析解答.
(3)根据题意,当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,是因为二氧化碳与水、碳酸钠溶液反应生成碳酸氢钠,进行分析解答.
(4)根据题意,20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g,结合二氧化碳与氢氧化钠反应生成碳酸钠和水,进行分析解答.
解答 解:(1)仪器a的名称是长颈漏斗;装置A中大理石或石灰石和稀盐酸反应来制取,属于固液常温型,同时生成氯化钙、水,反应的化学方程式是:CaCO3+2HCl=CaCl2+H2O+CO2↑.二氧化碳不能燃烧、不能支持燃烧,在b处检验是否有CO2逸出的操作是收集二氧化碳验满的方法为将燃着的木条放在导管口,木条熄灭,说明有气体逸出.
(2)装置C中放有干和湿的pH试纸各一张,当通入CO2一段时间后,湿pH试纸显示pH约为6,干pH试纸显示pH仍为7,是因为二氧化碳能与水反应生成碳酸,碳酸显酸性,说明了CO2与水反应后的溶液显酸性.
(3)当通入CO2一段时间后,装置D中观察到溶液中有白色沉淀(NaHCO3)出现,是因为二氧化碳与水、碳酸钠溶液反应生成碳酸氢钠,反应的化学方程式为:Na2CO3+CO2+H2O=2NaHCO3↓.
(4)20℃时,碳酸钠在乙醇中几乎不溶解,氢氧化钠在乙醇中的溶解度为17.3g.20℃时,碳酸钠、碳酸氢钠在水中的溶解度分别为21.8g和9.6g.当通入CO2一段时间后,二氧化碳与水反应生成碳酸钠和水,碳酸钠在乙醇中几乎不溶解,故装置E中观察到的实验现象是出现白色沉淀(或浑浊)反应的化学方程式是2NaOH+CO2=Na2CO3+H2O.
故答案为:(1)长颈漏斗;CaCO3+2HCl=CaCl2+H2O+CO2↑;将燃着的木条放在导气管口,观察木条是否熄灭;
(2)CO2与水反应后的溶液显酸性;
(3)Na2CO3+CO2+H2O=2NaHCO3↓;
(4)出现白色沉淀(或浑浊);2NaOH+CO2=Na2CO3+H2O.
点评 本题难度不大,是中考的重要考点之一,熟练掌握实验室中制取二氧化碳气体的反应原理、二氧化碳的化学性质等是正确解答本题的关键.

【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】小明用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的实验
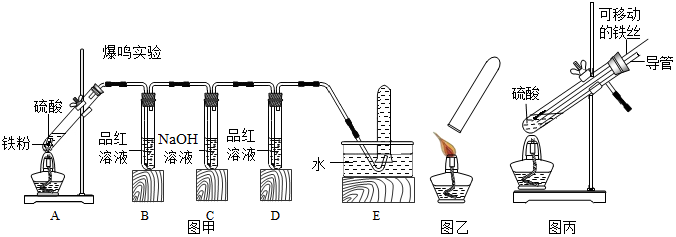
请帮助小明完成下表:
| A中硫酸的浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验三 | 25% | ③ | 不褪色 | ④ | 只有H2 |
【交流反思】(1)写出实验三中铁与硫酸溶液反应的化学方程式Fe+H2SO4═FeSO4+H2↑,
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因防止生成的气体从导管逸出
,该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸.
| A. | 分子 | B. | 阳离子 | C. | 阴离子 | D. | 原子 |
 学习化学一年后,同学们对课本上“支持燃烧的气体一般是氧气”这句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:
学习化学一年后,同学们对课本上“支持燃烧的气体一般是氧气”这句话产生了质疑.在老师的帮助下,用金属钠来探究下列问题:【提出问题】金属钠能否在其他气体(如:CO2)中燃烧?
【查阅资料】金属Na性质活泼,常温下,它极易与氧气反应生成白色固体氧化钠,氧化钠溶于水生成氢氧化钠.金属钠还可以与水剧烈反应放出氢气.
【实验探究】在实验室中,同学们发现金属钠保存在煤油中;
实验:将燃烧的钠迅速伸入盛有CO2的集气瓶中,观察到钠在CO2中继续燃烧,反应后冷却,瓶内附着黑色颗粒,并粘附着白色物质.
【问题讨论】
(1)金属钠保存在煤油中的原因是:钠的密度比煤油大,能使钠和空气隔绝.
(2)根据上述资料写出钠块投入水中发生反应的化学方程式:2Na+2H2O═2NaOH+H2↑.
(3)实验中生成的黑色颗粒是,而白色物质可能是什么呢?
①同学们围绕白色物质可能是什么产生如下猜想:甲认为白色物质是氧化钠,乙认为是碳酸钠,丙认为是氧化钠和碳酸钠的混合物,丁认为是氢氧化钠.
我认为丁的猜想是错误的,理由是反应物中不含有氢元素.
②对白色物质是什么进行实验再探究,方案设计如下:
| 实验操作 | 实验现象 | 实验结论 | |
| 方案1 | 取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入无色酚酞试液,观察 | 溶液变成红色 | 白色物质中一定有氧化钠 |
| 方案2 | 取该样品少量于试管里,滴加足量盐酸,观察 | 溶液中有气泡冒出 | 白色物质中一定有碳酸钠. |
| 方案3 | (1)取该样品少量于试管里,加入适量的水,振荡,过滤,向滤液中加入过量的氯化钙溶液溶液 (供选试剂:A.石灰水B.氯化钙溶液 C.硫酸铜溶液) (2)过滤,再向滤液里滴加无色酚酞试液. | 出现白色沉淀 无明显现象出现 | 乙(在甲、乙、丙中选)的猜想成立. |
【拓展应用】测定实验中使用的盐酸(如图)的实际质量分数.
为了测定,小明配制了20%的氢氧化钠溶液100g然后在烧杯中加入20g配得的氢氧化钠溶液,再逐滴加入该盐酸,恰好完全反应时测得消耗了25g该盐酸.
请以此次测定的数据,计算该盐酸的实际质量分数为14.6%,但发现测得的实际质量分数与标签上标出的质量分数不一致,可能原因部分氯化氢挥发出去(不考虑误差).
| A. | 甲溶液呈中性,乙溶液呈碱性 | |
| B. | 甲溶液属于酸性溶液,乙溶液属于碱性溶液 | |
| C. | 甲溶液一定是酸性溶液,乙溶液一定是碱性溶液 | |
| D. | 甲溶液使无色酚酞变红色,乙溶液不能使无色酚酞变色 |
| A. |  某温度下,向一定量不饱和硝酸钾溶液中不断加入硝酸钾晶体 | |
| B. |  向一定量的稀盐酸中逐滴滴加水 | |
| C. |  向一定量的氢氧化钠和碳酸钠的混合溶液中逐滴滴加盐酸 | |
| D. |  向一定量氯化铜溶液中加入一定量铝 |
