题目内容
10.A、B两种物质的溶解度曲线如图所示.下列说法中正确的是( )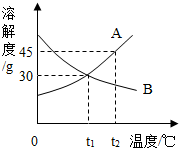
| A. | t1℃时A和B的溶解度相等 | |
| B. | t2℃时A和B的饱和溶液,降温到t1℃时两者仍是饱和溶液 | |
| C. | t2℃时在A的饱和溶液中加入少量水,A的溶解度变小 | |
| D. | t2℃时在100g水中加入40g A,可形成不饱和溶液 |
分析 A、溶解度曲线的交点表示该温度下物质的溶解度相等;
B、据AB的溶解度随温度变化情况分析解答;
C、温度不变,物质的溶解度不变;
D、据该温度下A的溶解度解答.
解答 解:A、t1℃时A和B的溶解度曲线交于一点,二者的溶解度相等,正确;
B、A的溶解度随温度降低而减小,B的溶解度随温度降低而增大,所以t2℃时A和B的饱和溶液,降温到t1℃时A仍饱和,B变为不饱和溶液,故错误;
C、温度不变,物质的溶解度不变,所以t2℃时在A的饱和溶液中加入少量水,A的溶解度不会改变,故错误;
D、t2℃时A的溶解度是45g,即100g水中最多溶解45g的A,所以在100g水中加入40g A,形成的是不饱和溶液,正确.
故选:AD.
点评 了解溶解度概念、溶解度曲线的意义等知识,才能结合题意灵活解答,能较好的考查学生分析、解决问题的能力.

练习册系列答案
相关题目
20.同学们利用硫酸、硝酸钡、氢氧化钠、碳酸钾四种物质的溶液进行探究学习.
【实验探究】如图所示,A、B、C、D四组同学分别进行了下列实验,请写出D中发生反应的化学方程式Ba(N03)2+K2CO3=BaCO3↓+2KNO3.
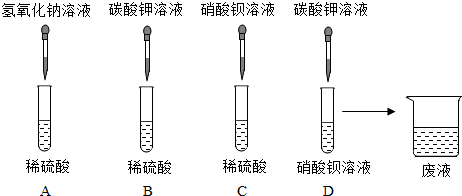
【实验结论】完成实验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀.向无色溶液中滴加紫色石蕊溶液,溶液变为红色.由此判断,产生的白色沉淀是BaSO4(或硫酸钡),废液中一定不含有的离子是OH-、CO${\;}_{3}^{2-}$.
【实验拓展】为验证该溶液中可能含有的离子是否存在,设计如下实验方案进行验证.
【实验探究】如图所示,A、B、C、D四组同学分别进行了下列实验,请写出D中发生反应的化学方程式Ba(N03)2+K2CO3=BaCO3↓+2KNO3.

【实验结论】完成实验后,四组同学将废液倒入同一个烧杯中,再将废液过滤,得到无色溶液和白色沉淀.向无色溶液中滴加紫色石蕊溶液,溶液变为红色.由此判断,产生的白色沉淀是BaSO4(或硫酸钡),废液中一定不含有的离子是OH-、CO${\;}_{3}^{2-}$.
【实验拓展】为验证该溶液中可能含有的离子是否存在,设计如下实验方案进行验证.
| 溶液中可能含有的离子 | 实验步骤 | 实验现象 | 实验结论 |
| 可能含有Ba2+ | 向滤液中滴加稀硫酸 | 产生白色沉淀 | 含有该离子 |
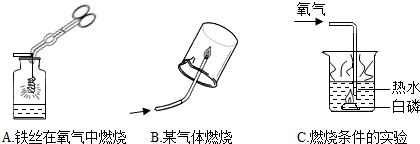
1.下列有关实验现象描述错误的是( )
| A. | 红磷在空气中燃烧产生大量白烟 | |
| B. | 硫在氧气中燃烧产生淡蓝色火焰 | |
| C. | 铁丝在氧气中剧烈燃烧,火星四射,生成一种黑色固体 | |
| D. | 食盐溶于水后溶液温度没有明显变化 |
5.下列措施或事故处理方法不正确的是( )
| A. | 用盐酸除去铁钉表面的铁锈 | |
| B. | 用甲醛浸泡海产品防止变质 | |
| C. | 炒菜时油锅着火,立即用锅盖盖灭 | |
| D. | 氢氧化钠溶液不慎沾在皮肤上,要用大量水冲洗,再涂上硼酸溶液 |
2.下列化学用语与所表述的意义相符的是( )
①2Ca2+--2个钙离子 ②O2--2个氧原子 ③2H2O--2个水分子
④2H--2个氢元素 ⑤$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
①2Ca2+--2个钙离子 ②O2--2个氧原子 ③2H2O--2个水分子
④2H--2个氢元素 ⑤$\stackrel{0}{{N}_{2}}$--氮气中氮元素的化合价为零.
| A. | ①④⑤ | B. | ②④ | C. | ①③⑤ | D. | ②③ |
19.自来水厂净水过程中,不需要进行的操作是( )
| A. | 蒸馏 | B. | 沉淀 | C. | 过滤 | D. | 吸附 |