题目内容
4.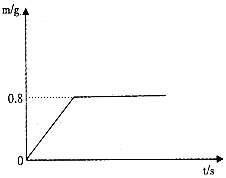 实验室用34g过氧化氢溶液和适量的二氧化锰混合制取氧气,生成氧气的质量与反应时间的关系如图所示(计算精确到小数点后两位)
实验室用34g过氧化氢溶液和适量的二氧化锰混合制取氧气,生成氧气的质量与反应时间的关系如图所示(计算精确到小数点后两位)(1)求过氧化氢中的氢元素质量分数
(2)反应生成氧气的质量为0.8g.
(3)计算实验中生成水的质量(精确到小数点后两位).
分析 根据题意和生成氧气的质量与反应时间的关系图,完全反应后生成氧气的质量为0.8g,据此根据反应的化学方程式计算出生成水的质量即可.
解答 解:(1)过氧化氢中氢元素的质量分数是$\frac{1×2}{1×2+16×2}$×100%=5.9%,故填:5.9%;
(2)由图象可知,完全反应后生成氧气的质量为0.8g;故填:0.8;
(3)解:设生成水的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
36 32
x 0.8g
$\frac{36}{x}=\frac{32}{0.8g}$
x=0.90g
答:实验中生成水的质量为0.90g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意(或图示信息)等各种信息是正确解答本题的前提和关键.

练习册系列答案
相关题目
12.下列气体中,能引起酸雨的是( )
| A. | CO | B. | CH4 | C. | SO2 | D. | NH3 |
19.在下列物质中氮元素的化合价为+5价的物质是( )
| A. | N2 | B. | N2O4 | C. | HNO3 | D. | NH3 |
9.“生命可贵,安全第一”下列做法或认识错误的是( )
| A. | 炒菜时油锅着火,应立即用锅盖盖灭 | |
| B. | 进入久未开启的菜窖,先用蜡烛做灯火实验 | |
| C. | 厨房煤气通道漏气,立即关闭阀门并开窗通风 | |
| D. | 矿井内充满瓦斯(主要成分是甲烷),马上点燃除去 |
16.生活中的下列变化,属于化学变化的是( )
| A. | 雪糕慢慢融化 | B. | 洗涤剂清晰油污 | ||
| C. | 久置的食物腐化 | D. | 敞口放置的雪碧慢慢减少 |
14.绿茶中的单宁酸具有抑制血压上升、清热解毒、抗癌等功效,其化学式为C76H52O46,下列说法不正确的是( )
| A. | 单宁酸分子中碳、氢、氧原子个数比为38:26:23 | |
| B. | 单宁酸属于有机物 | |
| C. | 单宁酸由碳、氢、氧三种元素组成 | |
| D. | 一个单宁酸分子中含26个氢分子 |