题目内容
4.6g常见的有机物A在空气中完全燃烧,产生二氧化碳8.8g,产生水蒸气5.4g
(1)有机物A的名称
(2)若有机物A不完全燃烧,只产生一氧化碳和水,请问此4.6g有机物A不完全燃烧最多能产生多少克有毒气体?
(1)有机物A的名称
(2)若有机物A不完全燃烧,只产生一氧化碳和水,请问此4.6g有机物A不完全燃烧最多能产生多少克有毒气体?
考点:质量守恒定律及其应用,化合物中某元素的质量计算
专题:化学用语和质量守恒定律
分析:根据二氧化碳的质量可以计算碳元素、氧元素的质量,根据水蒸气的质量可以计算氢元素、氧元素的质量,进一步可以判断有机物A的名称;
根据有机物的质量、反应的化学方程式可以计算产生一氧化碳的质量.
根据有机物的质量、反应的化学方程式可以计算产生一氧化碳的质量.
解答:解:(1)参加反应的氧气质量为:8.8g+5.4g-4.6g=9.6g,
8.8g二氧化碳中碳元素的质量为:8.8g×
×100%=2.4g,氧元素的质量为:8.8g-2.4g=6.4g,
5.4g水蒸气中氢元素的质量为:5.4g×
×100%=0.6g,氧元素的质量为:5.4g-0.6g=4.8g,
有机物A中氧元素的质量为:6.4g+4.8g-9.6g=1.6g,
有机物A中,碳原子、氢原子、氧原子的个数比为:
:
:
=2:6:1,即A的化学式是C2H5OH,是乙醇.
故填:乙醇.
(2)设生成一氧化碳的质量为x,
C2H5OH+2O2
2CO+3H2O,
46 56
4.6g x
=
,
x=5.6g,
答:最多能产生5.6g一氧化碳.
8.8g二氧化碳中碳元素的质量为:8.8g×
| 12 |
| 44 |
5.4g水蒸气中氢元素的质量为:5.4g×
| 2 |
| 18 |
有机物A中氧元素的质量为:6.4g+4.8g-9.6g=1.6g,
有机物A中,碳原子、氢原子、氧原子的个数比为:
| 2.4g |
| 12 |
| 0.6g |
| 1 |
| 1.6g |
| 16 |
故填:乙醇.
(2)设生成一氧化碳的质量为x,
C2H5OH+2O2
| ||
46 56
4.6g x
| 46 |
| 4.6g |
| 56 |
| x |
x=5.6g,
答:最多能产生5.6g一氧化碳.
点评:化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和,只是进行相关方面判断和计算的基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
日常生活 中下列做法属于化学变化的是( )
| A、用砂纸磨去铁片表面的铁锈 |
| B、给气球充入氢气 |
| C、桔子榨成汁 |
| D、用食醋去除水垢 |
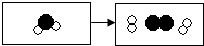 如图是密闭容器中某反应的微观示意图,“
如图是密闭容器中某反应的微观示意图,“ ”、“
”、“ ”表示不同种元素的原子.
”表示不同种元素的原子.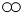 B.
B. C.
C.
 ”和“
”和“ ”两种原子的本质区别是
”两种原子的本质区别是 ”表示水分子,则MnO2催化“
”表示水分子,则MnO2催化“ ”分解的化学方程式为
”分解的化学方程式为 ”表示二氧化碳分子,写出“
”表示二氧化碳分子,写出“ ”与氧化铁反应的化学方程式
”与氧化铁反应的化学方程式 ”在此反应中体现
”在此反应中体现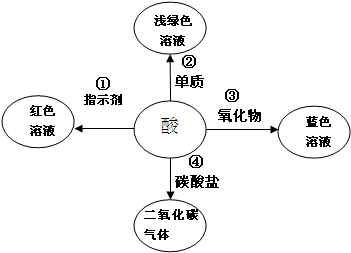 酸是很重要的物质,在初三化学学习中,很多化学实验都用到酸(盐酸和硫酸).酸能够跟很多种类的物质发生化学反应,如图是对酸的部分化学性质的归纳.
酸是很重要的物质,在初三化学学习中,很多化学实验都用到酸(盐酸和硫酸).酸能够跟很多种类的物质发生化学反应,如图是对酸的部分化学性质的归纳.