题目内容
材料的发展和应用,推动了社会的进步.铁、铜、棉花、聚乙烯塑料中人们生活和生产中常见的材料.
(1)铁是世界上使用最广的金属,工业上炼铁是利用一氧化碳的还原性把铁从铁的矿石中还原出来.请写出一氧化碳和氧化铁在高炉中的化学反应方程式 .
(2)为了探究铁和铜的金属活动性强弱,完成该实验有多种方案,写出其中一种方案中涉及的化学反应方程式 .
(1)铁是世界上使用最广的金属,工业上炼铁是利用一氧化碳的还原性把铁从铁的矿石中还原出来.请写出一氧化碳和氧化铁在高炉中的化学反应方程式
(2)为了探究铁和铜的金属活动性强弱,完成该实验有多种方案,写出其中一种方案中涉及的化学反应方程式
考点:铁的冶炼,金属活动性顺序及其应用,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)依据该反应的反应物生成物及条件结合化学方程式的书写要求书写即可;
(2)初中范围内能证明金属活动性强热的方法主要有a、与酸反应;b、金属与盐溶液的反应,据此设计实验并书写方程式即可.
(2)初中范围内能证明金属活动性强热的方法主要有a、与酸反应;b、金属与盐溶液的反应,据此设计实验并书写方程式即可.
解答:解:(1)一氧化碳和氧化铁在高炉中反应会生成铁与二氧化碳,其方程式为:3CO+Fe2O3
2Fe+3CO2;
(2)由于铁的金属活动性在氢前,而铜的金属活动性在氢后,所以可采用两者与稀硫酸反应的方法判断其金属活动性,能反应产生气泡的金属活动性强,不能反应的活动性较弱,也可采用铁与硫酸铜溶液反应,铁能置换出铜,所以金属的活动性铁>铜,涉及的方程式为:Fe+H2SO4=FeSO4+H2↑和Fe+CuSO4=Cu+FeSO4.
故答案为:(1)3CO+Fe2O3
2Fe+3CO2;(2)Fe+H2SO4=FeSO4+H2↑(或Fe+CuSO4=Cu+FeSO4合理即可).
| ||
(2)由于铁的金属活动性在氢前,而铜的金属活动性在氢后,所以可采用两者与稀硫酸反应的方法判断其金属活动性,能反应产生气泡的金属活动性强,不能反应的活动性较弱,也可采用铁与硫酸铜溶液反应,铁能置换出铜,所以金属的活动性铁>铜,涉及的方程式为:Fe+H2SO4=FeSO4+H2↑和Fe+CuSO4=Cu+FeSO4.
故答案为:(1)3CO+Fe2O3
| ||
点评:此题是一道多点知识考查题,涉及到铁的冶炼和金属活动性的验证等相关的问题,题目难度不大,是对学生基础知识掌握程度的验证.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
二氧化碳由碳、氧两种元素组成,这两种元素的本质区别是( )
| A、质子数不同 |
| B、中子数不同 |
| C、电子数不同 |
| D、相对原子质量不同 |
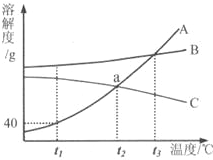 如图为A、B、C三种物质的溶解度曲线,据图回答:
如图为A、B、C三种物质的溶解度曲线,据图回答: 如图所示是A、B、C三种固体物质的溶解度曲线,请根据图示回答.
如图所示是A、B、C三种固体物质的溶解度曲线,请根据图示回答.