题目内容
氧化铜矿石含有CuO、Cu2(OH)2CO3和Fe2O3,还含有一些不溶于水、不溶于酸的其他杂质.铜、铁是畜禽所必需的微量元素.某饲料厂联合生产硫酸铜和硫酸铁工艺流程如下:(提示:溶液中当pH=3.8时硫酸铁全部转化为Fe(OH)3沉淀,pH=6.4时硫酸铜全部转化为Cu(OH)2沉淀)

(1)氧化铜矿石粉碎的目的是 .
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的化学方程式 .
(3)“中和/过滤”中加入CaCO3的目的是 .
(4)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有 .
(5)Fe(OH)3与硫酸反应的化学方程式 .
(6)“烘干粉碎”的实验结果如表所示.
硫酸铜晶体(CuSO4?5H2O)干燥实验表
表中,m为CuSO4?5H2O晶体的质量,x为干燥后所得晶体中结晶水的个数.据此可确定由CuSO4?5H2O脱水得流程中所示产品的适宜工艺条件分别为 、 (分别指出温度和时间).

(1)氧化铜矿石粉碎的目的是
(2)写出“酸浸”中Cu2(OH) 2CO3发生反应的化学方程式
(3)“中和/过滤”中加入CaCO3的目的是
(4)上述工艺流程中多处涉及“过滤”,实验室中过滤操作需要使用的玻璃仪器有
(5)Fe(OH)3与硫酸反应的化学方程式
(6)“烘干粉碎”的实验结果如表所示.
| 序号 | t/h | t/℃ | m/g | x |
| 1 | 3 | 80 | 5 | 4 |
| 2 | 3 | 160 | 10 | 1 |
| 3 | 4 | 160 | 10 | 0.8 |
| 4 | 4 | 160 | 5 | 0 |
| 5 | 5 | 80 | 5 | 3 |
表中,m为CuSO4?5H2O晶体的质量,x为干燥后所得晶体中结晶水的个数.据此可确定由CuSO4?5H2O脱水得流程中所示产品的适宜工艺条件分别为
考点:物质的相互转化和制备,过滤的原理、方法及其应用,酸的化学性质,盐的化学性质,书写化学方程式、文字表达式、电离方程式
专题:物质的制备
分析:(1)根据反应物的接触面积与反应速率成正比进行分析;
(2)根据碱式碳酸铜和稀硫酸反应会生成硫酸铜、水和二氧化碳进行分析;
(3)根据碳酸钙和酸反应会使溶液酸性降低,利于铁生成氢氧化铁沉淀进行分析;
(4)根据过滤需要的仪器和各仪器的作用选取仪器;
(5)根据氢氧化铁会与硫酸发生中和反应进行分析;
(6)根据表2、图1产物与温度、时间的关系进行分析.
(2)根据碱式碳酸铜和稀硫酸反应会生成硫酸铜、水和二氧化碳进行分析;
(3)根据碳酸钙和酸反应会使溶液酸性降低,利于铁生成氢氧化铁沉淀进行分析;
(4)根据过滤需要的仪器和各仪器的作用选取仪器;
(5)根据氢氧化铁会与硫酸发生中和反应进行分析;
(6)根据表2、图1产物与温度、时间的关系进行分析.
解答:解:(1)反应物的接触面积与反应速率成正比,将氧化铜矿石粉碎,增大了反应物的接触面积,加快了反应速率,氧化铜矿石粉碎的目的是:增大反应物的接触面积,加快化学反应速率;
(2)碱式碳酸铜和稀硫酸反应生成硫酸铜、水和二氧化碳,
化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)碳酸钙和酸反应生成盐和水,降低了溶液的酸性,从而时铁离子水解生成沉淀而除去,所以“中和/过滤”中加入CaCO3的目的是:适当降低溶液的酸性,使Fe3+水解成沉淀而除出;
(4)实验室中过滤操作需要使用的玻璃仪器有盛放溶液的烧杯,起引流作用的玻璃棒,过滤作用的漏斗,所以实验室中过滤操作需要使用的玻璃仪器有:烧杯、玻璃棒、漏斗;
(5)氢氧化铁和硫酸反应生成硫酸铁和水,化学方程式为:2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O;
(6)由CuSO4?5H2O脱水得CuSO4?H2O结合表2知,要想得到目标产物,适宜的温度和时间分别是160℃、3h.
故答案为:(1)增大反应物的接触面积,加快化学反应速率;
(2)Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)适当降低溶液的酸性,使Fe3+水解成沉淀而除出;
(4)烧杯、玻璃棒、漏斗;
(5)2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O;
(6)160℃、3h.
(2)碱式碳酸铜和稀硫酸反应生成硫酸铜、水和二氧化碳,
化学方程式为:Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)碳酸钙和酸反应生成盐和水,降低了溶液的酸性,从而时铁离子水解生成沉淀而除去,所以“中和/过滤”中加入CaCO3的目的是:适当降低溶液的酸性,使Fe3+水解成沉淀而除出;
(4)实验室中过滤操作需要使用的玻璃仪器有盛放溶液的烧杯,起引流作用的玻璃棒,过滤作用的漏斗,所以实验室中过滤操作需要使用的玻璃仪器有:烧杯、玻璃棒、漏斗;
(5)氢氧化铁和硫酸反应生成硫酸铁和水,化学方程式为:2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O;
(6)由CuSO4?5H2O脱水得CuSO4?H2O结合表2知,要想得到目标产物,适宜的温度和时间分别是160℃、3h.
故答案为:(1)增大反应物的接触面积,加快化学反应速率;
(2)Cu2(OH)2CO3+2H2SO4=2CuSO4+3H2O+CO2↑;
(3)适当降低溶液的酸性,使Fe3+水解成沉淀而除出;
(4)烧杯、玻璃棒、漏斗;
(5)2Fe(OH)3+3H2SO4=Fe2(SO4)3+6H2O;
(6)160℃、3h.
点评:本题考查了制备实验方案设计,涉及知识点较多,明确物质的性质是解本题关键,难点是(6)中温度和时间的选取,明确图表的含义即可得出正确结论,同时考查学生分析问题和解决问题的能力,难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
下列图象能正确反映其对应操作中各量变化关系的是( )
A、 用一定质量的高锰酸钾加热制氧气 |
B、 向一定质量的石灰石中加入过量的稀盐酸 |
C、 向一定温度下的饱和氢氧化钙溶液中不断加入氧化钙固体 |
D、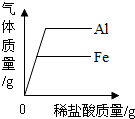 分别向等质量的铝和铁中加入溶质质量分数相同的稀盐酸至过量 |
下列属于化学变化的是( )
| A、汽油挥发 | B、粮食酿酒 |
| C、水结成冰 | D、石墨导电 |
甲基咪唑是一种微黄色的固体,化学式为C4H6N2,下列关于它的说法正确的是( )
| A、该物质中碳、氢、氮三种元素的质量比为4:6:2 |
| B、该物质是由4个碳原子、6个氢原子、2个氮原子构成 |
| C、该物质是由分子构成,每个分子由碳、氢、氮三种元素组成 |
| D、该物质中碳元素的质量分数约为58.5% |
 如图为四种粒子的结构示意图,完成以下填空:
如图为四种粒子的结构示意图,完成以下填空: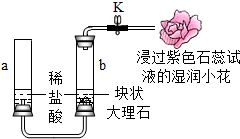 某实验小组用如图装置研究CO2的性质.提示:
某实验小组用如图装置研究CO2的性质.提示:
