题目内容
15.空气是一种重要的资源.(1)空气中含量较多且化学性质不活泼的气体是氮气.
(2)同温同压下,气体的体积比等于分子数目比.若空气中其它成分忽略不计,图1中可表示空气微观模型的是C(填序号).
(3)利用空气可以制取促进农作物生长的肥料.其生产流程如图2:
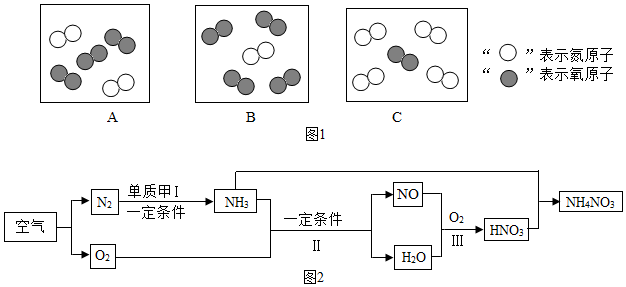
①甲物质是H2(或氢气).
②上述Ⅰ~Ⅳ的化学反应中属于化合反应的有3个,反应Ⅲ的化学方程式为4NO+3O2+2H2O=4HNO3,其中化合价升高是氮元素.
③最终制得的NH4NO3属于N肥.
分析 (1)根据空气各成分的性质进行分析判断;(2)根据空气的组成解答;(3)根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:(1)空气的成分按体积计算,大约是:氮气占78%、氧气占21%,氧气的化学性质比较活泼,氮气化学性质稳定,因此空气中含量较多且化学性质不活泼的气体是氮气;
(2)氧气约占空气体积的五分之一,氮气约占空气体积的五分之四,图中可表示空气微观模型的是C;
(3)①氮气和甲反应生成了氨气,根据质量守恒定律可知甲物质为 H2 (或氢气).
②Ⅰ是氮气和氢气生成氨气,属于化合反应;Ⅱ是氨气和氧气在催化剂、高温、高压下生成一氧化氮和水,不属于化合反应;Ⅲ是一氧化氮、氧气和水反应生成硝酸,属于化合反应;Ⅳ是氨气和硝酸反应生成硝酸铵,属于化合反应;反应Ⅲ的化学方程式为一氧化氮、氧气、水反应生成硝酸,方程式是:
4NO+3O2+2H2O=4HNO3;氮元素化合价由+2到+5;
③在整个过程中化学肥料的三大元素N、P、K只出现了N,所以最终制得的化肥属于 N肥.
故答案为:
(1)氮气;(2)C;(3)①H2 (或氢气);②3;4NO+3O2+2H2O=4HNO3;氮;③N.
点评 解答本题关键是熟悉空气的组成,知道空气中各成分体积分数和性质用途,熟悉化学方程式的书写方法.

练习册系列答案
相关题目
5.近期有关民生热词:“舌尖上的安全”,下列做法符合食品安全要求的是( )
| A. | 用甲醛溶液浸泡海产品 | |
| B. | 为了使粽叶鲜亮,用硫酸铜溶液浸泡粽叶 | |
| C. | 用食盐腌制鸭蛋 | |
| D. | 用霉变花生榨食用油 |
6.Mg(OH)2是一种新型的阻燃剂,在温度达到380℃时分解吸收热量并释放出水,同时生成的氧化镁附着于可燃物的表面阻止了进一步燃烧.
(1)工业上常用氯化镁与碱反应得到Mg(OH)2,常用的碱有氨水和烧碱,写出烧碱制取Mg(OH)2的化学方程式2NaOH+MgCl2═2NaCl+Mg(OH)2↓.
(2)某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往一定量的氯化美中加入氯水(氨水易挥发),生成Mg(OH)2,再通过结晶、过滤,得到Mg(OH)2晶体.为探究获得较高Mg(OH)2晶体转化率的条件,该同学进行下述对比实验,数据如下:
①实验b和c的目的是探究氯化镁溶液浓度相同时,比较温度对Mg(OH)2转化率的影响.
②由实验数据可知,能够得到最多Mg(OH)2的条件是40g•L-1和40℃.
③在氯化镁溶液浓度都是40g•L-1的情况下,60℃时Mg(OH)2的转化率比40℃时低的原因是氨水易挥发,温度越高,氨水挥发越快,参与反应的氨水越少,获得的Mg(OH)2晶体越少.
(3)根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是②③(填编号).
①清除可燃物 ②使温度降低到着火点以下 ③隔绝空气.
(1)工业上常用氯化镁与碱反应得到Mg(OH)2,常用的碱有氨水和烧碱,写出烧碱制取Mg(OH)2的化学方程式2NaOH+MgCl2═2NaCl+Mg(OH)2↓.
(2)某同学用氨水在实验室模拟制取Mg(OH)2的过程:一定温度下,往一定量的氯化美中加入氯水(氨水易挥发),生成Mg(OH)2,再通过结晶、过滤,得到Mg(OH)2晶体.为探究获得较高Mg(OH)2晶体转化率的条件,该同学进行下述对比实验,数据如下:
| 实验编号 | 氯化镁溶液浓度/g•L-1 | 反应温度/℃ | Mg(OH)2转化率/% |
| a | 20 | 30 | 27.06 |
| b | 40 | 30 | 56.77 |
| c | 40 | 40 | 69.64 |
| d | 40 | 60 | 54.30 |
| e | 60 | 60 | 50.60 |
②由实验数据可知,能够得到最多Mg(OH)2的条件是40g•L-1和40℃.
③在氯化镁溶液浓度都是40g•L-1的情况下,60℃时Mg(OH)2的转化率比40℃时低的原因是氨水易挥发,温度越高,氨水挥发越快,参与反应的氨水越少,获得的Mg(OH)2晶体越少.
(3)根据燃烧的条件可知,Mg(OH)2能做阻燃剂的原因是②③(填编号).
①清除可燃物 ②使温度降低到着火点以下 ③隔绝空气.
10.下列实验现象的描述中,正确的是( )
| A. | 硫在空气中燃烧,发出明亮的蓝紫色火焰 | |
| B. | 铁锈与稀盐酸反应后,溶液由无色变成了浅绿色 | |
| C. | 向氢氧化钠溶液中滴加紫色石蕊溶液,溶液变红 | |
| D. | 碳高温还原氧化铜时,黑色粉末逐渐变为亮红色 |
7.如图实验操作中正确的是( )
| A. | 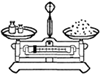 用天平称食盐 | B. | 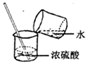 稀释浓硫酸 | C. | 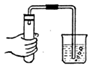 检查气密性 | D. | 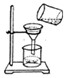 过滤 |
4.发展绿色食品,避免“白色污染”是保护环境、提高人类生存质量的主要措施,产生“白色污染”的是( )
| A. | 空气污染物 | B. | 白色废弃物 | C. | 塑料 | D. | 工业上的“三废” |
5.下列化学方程式书写正确的是( )
| A. | 氧化汞加热分解:HgO$\frac{\underline{\;\;△\;\;}}{\;}$Hg+O2↑ | |
| B. | 铁在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | |
| C. | 铁片投入稀盐酸中:2Fe+6HCl=2 FeCl3+3H2↑ | |
| D. | 碳在氧气中燃烧:C+O2=CO2 |
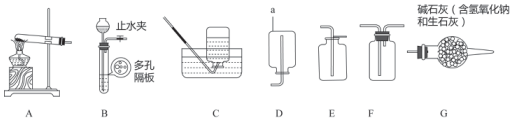
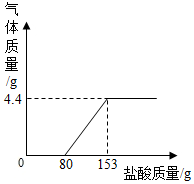 现有一包Na2CO3和NaOH固体样品,为了测定Na2CO3的质量分数,取该样品20g,加水搅拌至全部溶解.然后逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示
现有一包Na2CO3和NaOH固体样品,为了测定Na2CO3的质量分数,取该样品20g,加水搅拌至全部溶解.然后逐滴加入稀盐酸至过量,测得生成气体质量与所加稀盐酸质量关系如图所示