题目内容
8.金属钴的部分性质如表所示,根据表中的信息回答下列问题.(CoCl2溶液是粉红色的)| 颜色状态 | 硬度 | 熔点 | 化学性质 |
| 银白色固体 | 硬 | 1495℃ | 能与稀盐酸反应 |
(2)请自选实验器材和试剂设计实验,比较金属钴与金属锌的活动性强弱,完成如表.
| 实验操作 | 实验现象 | 实验结论 |
| 将打磨过的钴片放入硫酸锌溶液中 | 无明显现象 | 金属锌比金属钴活泼 |
分析 (1)根据钴和稀盐酸反应会生成氯化钴和氢气进行分析;
(2)根据金属活动性顺序进行分析.
解答 解:(1)钴和稀盐酸反应会生成氯化钴和氢气,实验现象为:金属不断溶解,表面产生气泡,溶液由无色变为粉红色;
(2)
| 实验操作 | 实验现象 | 实验结论 |
| 将打磨过的钴片放入硫酸锌溶液中 | 无明显现象 | 金属锌比金属钴活泼 |
(2)
| 实验操作 | 实验现象 | 实验结论 |
| 将打磨过的钴片放入硫酸锌溶液中 | 无明显现象 |
点评 本题主要考查了金属活动性顺序的应用,难度不大,注意在平时加强训练即可完成.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
16.纯金属很难满足生产和生活中的各种特殊要求.因此,人们在生产实践中制造出了许许多多具有特殊性能的“新型金属”--合金.下列关于合金的说法正确的有( )
①合金中一定不含非金属元素
②合金的制作过程中发生了化学变化
③合金中一定含有金属
④合金一定是混合物
⑤一般来说,日常使用的金属材料,大多数属于合金.
①合金中一定不含非金属元素
②合金的制作过程中发生了化学变化
③合金中一定含有金属
④合金一定是混合物
⑤一般来说,日常使用的金属材料,大多数属于合金.
| A. | ①② | B. | ②③ | C. | ②③⑤ | D. | ③④⑤ |
3.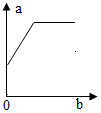 在20℃时,向100g不饱和的氯化铵溶液中逐渐加入氯化铵固体,且a、b的关系如图所示.则下列选项正确的是( )
在20℃时,向100g不饱和的氯化铵溶液中逐渐加入氯化铵固体,且a、b的关系如图所示.则下列选项正确的是( )
 在20℃时,向100g不饱和的氯化铵溶液中逐渐加入氯化铵固体,且a、b的关系如图所示.则下列选项正确的是( )
在20℃时,向100g不饱和的氯化铵溶液中逐渐加入氯化铵固体,且a、b的关系如图所示.则下列选项正确的是( )| A. | a--溶解度,b--溶质质量 | B. | a--温度,b--溶质质量 | ||
| C. | a--溶质质量,b--时间 | D. | a--溶解度,b--溶剂质量 |
20.下列化学实验不能实现实验目的是( )
| A. | 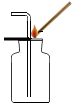 二氧化碳验满 | |
| B. | 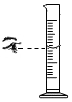 量取3mL液体 | |
| C. | 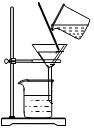 过滤浑浊的河水 | |
| D. | 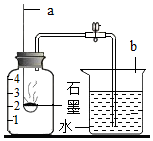 用石墨来测定空气中 氧气的含量 |
17.我国一些大城市时不时地遭遇灰霾天气,灰霾天气是由空气中细颗粒物的含量增多造成的,它比粗颗粒物对能见度的影响更大.下列情况能直接造成灰霾天气的是( )
| A. | 焚烧垃圾 | B. | 随意丢弃所料 | C. | 随意丢弃废电池 | D. | 利用清洁能源 |

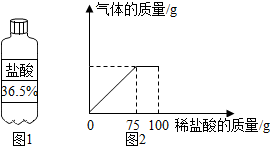 (1)配制溶质质量分数为7.3%的稀盐酸.
(1)配制溶质质量分数为7.3%的稀盐酸.