题目内容
11.小新同学用20g含碳酸钠53%的天然碱,制取氢氧化钠用于制作“叶脉书签”(杂质不参加反应).操作过程如下:
请计算:(1)20g样品中碳酸钠的质量.
(2)反应后所得滤液中氢氧化钠的质量分数为多少?
分析 碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,根据反应的化学方程式及其提供的数据可以进行相关方面的计算.
解答 解:(1)20g样品中碳酸钠的质量为:20g×53%=10.6g,
答:20g样品中碳酸钠的质量为10.6g.
(2)设反应生成氢氧化钠质量为x,
Na2CO3+Ca(OH)2═CaCO3↓+2NaOH,
106 80
10.6g x
$\frac{106}{10.6g}$=$\frac{80}{x}$,
x=8g,
反应后所得滤液中氢氧化钠的质量分数为:$\frac{8g}{200g}$×100%=4%,
答:反应后所得滤液中氢氧化钠的质量分数为4%.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.如图,甲和乙分别是氢气和一氧化碳还原氧化铜的实验,下列有关说法正确的是( )
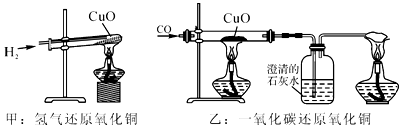

| A. | 甲实验试管口向下倾斜可防止生成的水倒流,也有利于将试管内的空气完全排出 | |
| B. | 乙实验只能通过澄清石灰水是否变浑浊判断反应是否发生 | |
| C. | 甲、乙两实验中,都应先使试管、玻璃管均匀受热,再通入气体,以防止发生爆炸 | |
| D. | 甲、乙两实验中,氢气和一氧化碳都将氧化铜变成游离态的铜,都发生了置换反应 |
6.2017年4月22日江淮晨报讯,我省“两淮”地区发现巨大天然气矿藏,预测达1.9万亿立方米,天然气的主要成分是甲烷(化学式为CH4).下列说法正确的是( )
| A. | 天然气是混合物 | |
| B. | 甲烷是由一个碳原子和四个氢原子构成的 | |
| C. | 甲烷是由两种非金属组成的 | |
| D. | 甲烷中碳氢元素的质量比为1:4 |
16.分类、归纳、分析、推理等是化学学习中常用的思想和方法.下列相关说法不正确的是( )
| A. | 分类:生铁、天然气、冰水混合物都属于混合物 | |
| B. | 归纳:酸和碱中和一定都含有氢元素 | |
| C. | 分析:金刚石和石墨物理性质差异很大,是因为碳原子的排列方式不同 | |
| D. | 推理:碱性溶液能使物色酚酞变红,所以能使酚酞变红的溶液pH一定大于7 |
3.下列几种离子分别在HCl、KOH、BaCl2三种溶液中都能存在的是( )
| A. | OH- | B. | Na+ | C. | SO42- | D. | Mg2+ |
4.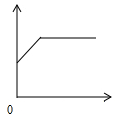 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )
 下列各选项与如图所示曲线相符的是( )
下列各选项与如图所示曲线相符的是( )| 选项 | 实验操作 | 横坐标 | 纵坐标 |
| A | 向一定质量的锌粉中加入稀硫酸 | 加入稀硫酸的质量/g | 生成氢气的质量/g |
| B | 向一定质量的硝酸银溶液中加入铜粉 | 加入铜粉的质量/g | 溶液的质量/g |
| C | 向一定质量的稀盐酸中不断加入碳酸钙粉末 | 加入碳酸钙的质量/g | 溶液的质量/g |
| D | 向氯化钠饱和溶液中加入水 | 加入水的质量/g | 溶质的质量/g |
| A. | A | B. | B | C. | C | D. | D |
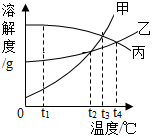 甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答下列问题:
甲、乙、丙三种固体物质的溶解度曲线如图所示,请回答下列问题: 请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站,“2-5号站”各站的对应物质属于不同类别的纯净物.
请同学们搭乘“化学地铁”一起畅游物质世界吧!如图所示,列车上的物质可与各站的对应物质发生一步进行的反应,方可驶向下一站,“2-5号站”各站的对应物质属于不同类别的纯净物.