题目内容
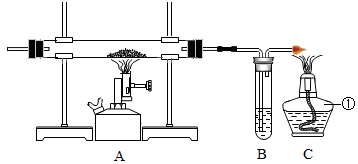
1.已知材料:在实验室里,金属钠保存在煤油中.在烧杯中加一些水,滴入几滴酚酞试液,然后把一小块钠放入水中,钠与水剧烈反应,钠熔为小球并在水面快速游动,产生一种可燃性气体,烧杯中的液体变红.请回答下列问题:
(1)钠、煤油、水三者的密度大小顺序为水>钠>煤油.
(2)钠与水反应的化学方程式为2Na+2H2O=2NaOH+H2↑.
分析 物质在化学变化中表现出来的性质叫化学性质,如可燃性、助燃性、氧化性、还原性等;物质不需要发生化学变化就表现出来的性质,叫物理性质;由题目的信息可知:在实验室里,金属钠保存在煤油中,因此钠的密度比煤油大;钠与水剧烈反应,钠熔为小球并在水面快速游动,因此水的密度比钠大;钠、煤油、水三者的密度大小顺序为:水>钠>煤油;钠与水剧烈反应生成氢氧化钠和氢气,配平即可.
解答 解:(1)由题目的信息可知:在实验室里,金属钠保存在煤油中,因此钠的密度比煤油大;钠与水剧烈反应,钠熔为小球并在水面快速游动,因此水的密度比钠大;钠、煤油、水三者的密度大小顺序为:水>钠>煤油;故答案为:水 钠 煤油;
(2)钠与水剧烈反应生成氢氧化钠和氢气,配平即可;故答案为:2Na+2H2O=2NaOH+H2↑;
点评 本考点考查了物质密度的大小和化学方程式的书写等,要记忆有关物质的性质,并能够在比较的基础上进行应用,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
11.通过下列实验操作和现象能得出相应结论的是( )
| 实验操作 | 现象 | 结论 | |
| A | 向收集满CO2的软塑料瓶中加入约1/3体积的紫色石蕊溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪且紫色石蕊变红 | CO2能与石蕊反应 |
| B | 50℃时,将17gKCl固体加入50g蒸馏水中,完全溶解后缓慢降温 | 降温至20℃时开始有晶体析出 | 20℃时,KCl的溶解度为17g |
| C | 将白磷浸没在热水中,再向热水中的白磷通氧气 | 通氧气前白磷不燃烧,通氧气后白磷燃烧 | 氧气是燃烧需要的条件之一 |
| D | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是CH4 |
| A. | A | B. | B | C. | C | D. | D |
12.四会生产的翡翠是人们喜爱的一种装饰品,翡翠的主要成份是硬玉[化学式为NaAl(Si2O6)].下列有关说法正确的是( )
| A. | 翡翠是一种纯净物 | B. | 硬玉含有10个原子 | ||
| C. | 硅元素的化合价为+4价 | D. | 翡翠由钠、铝、硅、氧四种元素构成 |
7.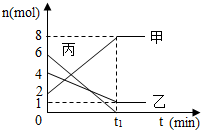 容器中含有甲、乙、丙三种物质,在一定条件下发生化学反应.甲、乙、丙的物质的量(n)随着反应时间(t)的变化如图所示.有关说法正确的是( )
容器中含有甲、乙、丙三种物质,在一定条件下发生化学反应.甲、乙、丙的物质的量(n)随着反应时间(t)的变化如图所示.有关说法正确的是( )
 容器中含有甲、乙、丙三种物质,在一定条件下发生化学反应.甲、乙、丙的物质的量(n)随着反应时间(t)的变化如图所示.有关说法正确的是( )
容器中含有甲、乙、丙三种物质,在一定条件下发生化学反应.甲、乙、丙的物质的量(n)随着反应时间(t)的变化如图所示.有关说法正确的是( )| A. | 该反应生成8mol甲 | |
| B. | 甲一定是化合物 | |
| C. | 该反应为分解反应 | |
| D. | 参加反应的乙和丙的物质的量之比为2:3 |
4.高铁酸钾(K2FeO4)是一种新型、高效的多功能水处理剂,受热时发生如下反应4K2FeO4$\frac{\underline{\;\;△\;\;}}{\;}$aR+4K2O+3O2↑,则aR是( )
| A. | 4FeO | B. | 2Fe2O3 | C. | 3F e2O3 | D. | 1 F e3O4 |
5.下列变化属于化学变化的是( )
| A. | 酒精挥发 | B. | 冰雪融化 | C. | 白磷自然 | D. | 瓷碗破碎 |