题目内容
14.已知某抗酸药主要成分为“氢氧化铝”,能和胃酸(主要成分为盐酸)发生中和反应,治疗胃酸过多症,一片该抗酸药实含氢氧化铝234mg.请计算:(1)Al(OH)3的相对分子质量为78
(2)片该抗酸药可消耗7.3%的盐酸多少克?(请写出计算过程).
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)欲正确解答本题,需根据化学方程式得出各物质之间的质量比,列出比例式计算即可.
解答 解:(1)氢氧化铝Al(OH)3的相对分子质量是27+(16+1)×3=78;
故答案为:78;
(2)每片该抗酸药实含氢氧化铝的质量=234mg=0.234g.
设可消耗7.3%的盐酸的质量为x.
Al(OH)3+3HCl═AlCl3+3H2O
78 109.5
0.234g x×7.3%
$\frac{78}{0.234g}=\frac{109.5}{x×7.3%}$
x=4.5g
答:可消耗7.3%的盐酸的质量为4.5g.
点评 本题难度不大,考查同学们结合标签新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
2.以下四组离子,有一组能大量共存且能形成无色透明溶液,它应该是( )
| A. | Fe3+ SO42- H+ Cl- | B. | Mg2+ Cl- OH- Na+ | ||
| C. | H+ Na+ K+ NO3- | D. | H+ Ba2+ NO3- SO42- |
9.Ⅰ.用一种试剂一次鉴别出下列各组物质的溶液,将选择的试剂的名称或化学式填入横线
(1)氢氧化钠、氯化钠、盐酸紫色石蕊试液
(2)氯化钠、硫酸钠、氯化铵氢氧化钡溶液
(3)盐酸、氢氧化钙、氢氧化钠碳酸钠溶液
Ⅱ.除去下列物质中的少量杂质,写出所选用的试剂和操作方法
Ⅲ.植物生长需要养分,土壤所能提供的养分是有限的,因此要靠施肥来补充.现有三种化肥:硫酸钾、磷矿粉、氯化铵,属于氮肥的是氯化铵;如何将该化肥与其它两种化肥区别开?请完成表格
(1)氢氧化钠、氯化钠、盐酸紫色石蕊试液
(2)氯化钠、硫酸钠、氯化铵氢氧化钡溶液
(3)盐酸、氢氧化钙、氢氧化钠碳酸钠溶液
Ⅱ.除去下列物质中的少量杂质,写出所选用的试剂和操作方法
| 物质(括号内为杂质) | 试剂 | 操作方法 |
| CuO(C) | ||
| 氯化钠固体(泥沙) | ||
| FeCl2溶液(CuCl2) |
| 实验步骤 | 现象 | 结论 |
| 步骤1:观察外观 | 灰色粉末 | 磷矿粉 |
| 步骤2:取另两种化肥少量,加入氢氧化钙溶液 | 有刺激性气味的气体产生 | 该化肥是氯化铵 |
19.下列物质可以由金属与酸反应制得的是( )
| A. | 氯化银 | B. | 硫酸锌 | C. | 氯化铁 | D. | 硫酸铜 |
6.要验证铜、银、铁三种金属活动性顺序时,不能选用哪组物质进行实验( )
| A. | 银、铜、硝酸亚铁 | B. | 银、铜、铁、硫酸铜 | ||
| C. | 银、铁、硫酸铜 | D. | 铜、硝酸亚铁、硝酸银 |
3.高铁酸钠(Na2FeO4)是一种新型高效的水处理剂.下列有关高铁酸钠的说法正确的是( )
| A. | 其相对原子质量为165 | |
| B. | 其中钠、铁、氧三种元素质量比是2:1:4 | |
| C. | 其一个分子中含有7个原子 | |
| D. | 其中铁元素的质量分数为27.71% |
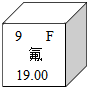 如图所示是氟元素在元素周期表中的相关信息,请回答下列问题:
如图所示是氟元素在元素周期表中的相关信息,请回答下列问题: