题目内容
(2003?天津)某同学设计了测定空气中氧气含量的实验,实验装置如图所示:该同学的实验步骤如下: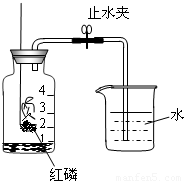
①将图中的集气瓶分为5等份,并做好标记.
②在带橡皮塞和导管的燃烧匙内装入足量的红磷,将导管上的止水夹夹紧,在酒精灯上点燃红磷,并立即伸入集气瓶内,塞紧橡皮塞.
③充分反应后,待集气瓶冷却至室温,打开止水夹.
请回答下列问题:
(1)该实验中红磷须稍过量,目的是;
(2)步骤③中,打开止水夹后观察到的现象是,由此可得出空气中氧气的体积分数约为.
(3)磷在空气中燃烧生成的氧化物通常可做强干燥剂.已知在标准状况下,32g氧气的体积是22.4L.在该条件下,制备71g这种干燥剂所消耗的空气的体积约为 L.
【答案】分析:只要熟悉用红磷测定空气里氧气含量的实验现象与实验原理,就能够得出本题的正确答案.原理是利用红磷燃烧,消耗氧气,产生内外压强差,冷却后打开止水夹,水沿导管流入集气瓶中,占据氧气的空间,根据流入水的多少,判断氧气的含量.因此红磷的量要充足,才能把氧气耗尽.因氧气约占空气体积的 ,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.第(3)需要根据磷燃烧的化学方程式,计算出制备71g五氧化二磷需要多少氧气,然后根据氧气在空气中所占体积分数计算出空气的体积.
,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.第(3)需要根据磷燃烧的化学方程式,计算出制备71g五氧化二磷需要多少氧气,然后根据氧气在空气中所占体积分数计算出空气的体积.
解答:解:(1)实验的目的是测定空气中氧气含量,原理是消耗氧气使装置内外产生压强差,水被吸入占据氧气的空间,从而达到测定氧气的目的.红磷过量,可使集气瓶中的氧气完全消耗.
(2)充分反应后,待集气瓶冷却至室温,集气瓶内外产生压强差,打开止水夹,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.由此可得出空气中氧气的体积分数约为 .
.
(3)设制备71g五氧化二磷需要氧气质量为X
4P+5O2 2P2O5
2P2O5
160 284
X 71g
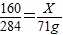
解得:X=40g
40g氧气的体积为: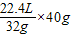 ═28L
═28L
消耗空气的体积为:28L÷ ═140L
═140L
故答案为:(1)使集气瓶中的氧气完全消耗.
(2)烧杯内的水沿导管流入集气瓶中,液面大约在标记1处; 1/5
(3)140L
点评:熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.
 ,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.第(3)需要根据磷燃烧的化学方程式,计算出制备71g五氧化二磷需要多少氧气,然后根据氧气在空气中所占体积分数计算出空气的体积.
,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.第(3)需要根据磷燃烧的化学方程式,计算出制备71g五氧化二磷需要多少氧气,然后根据氧气在空气中所占体积分数计算出空气的体积.解答:解:(1)实验的目的是测定空气中氧气含量,原理是消耗氧气使装置内外产生压强差,水被吸入占据氧气的空间,从而达到测定氧气的目的.红磷过量,可使集气瓶中的氧气完全消耗.
(2)充分反应后,待集气瓶冷却至室温,集气瓶内外产生压强差,打开止水夹,烧杯内的水沿导管流入集气瓶中,液面大约在标记1处.由此可得出空气中氧气的体积分数约为
 .
.(3)设制备71g五氧化二磷需要氧气质量为X
4P+5O2
 2P2O5
2P2O5160 284
X 71g
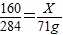
解得:X=40g
40g氧气的体积为:
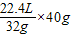 ═28L
═28L消耗空气的体积为:28L÷
 ═140L
═140L故答案为:(1)使集气瓶中的氧气完全消耗.
(2)烧杯内的水沿导管流入集气瓶中,液面大约在标记1处; 1/5
(3)140L
点评:熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目

