题目内容
9. 根据图中的信息判断,下列说法错误的是( )
根据图中的信息判断,下列说法错误的是( )| A. | 氟元素的相对原子质量为19.00 | |
| B. | 氟元素位于周期表第二周期 | |
| C. | 在化学反应中,氟原子较易得到电子 | |
| D. | 当x=8时,该微粒为阳离子 |
分析 A、图中元素周期表可以获得的信息:汉字下面的数字表示相对原子质量,据此进行分析判断.
B、根据周期数=原子核外电子层数,进行分析判断.
C、若原子的最外层电子数≥4,在化学反应中易得电子,若最外层电子数<4,在化学反应中易失去电子.
D、当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
解答 解:A、根据元素周期表中的一格可知,汉字下面的数字表示相对原子质量,元素的相对原子质量为19.00,故选项说法正确.
B、由氟的结构示意图,原子核内有9个质子,第一层上有2个电子,第二层上应有7个电子,核外有2个电子层;周期数=原子核外电子层数,则氟元素位于周期表第二周期,故选项说法正确.
C、由氟的结构示意图,原子核内有9个质子,第一层上有2个电子,最外层上应有7个电子,在化学反应中易得到1个电子而形成阴离子,故选项说法正确.
D、当x=8时,质子数=9,核外电子数=2+8=10,质子数<核外电子数,为阴离子,故选项说法错误.
故选:D.
点评 本题难度不大,灵活运用元素周期表中元素的信息(原子序数、元素符号、元素名称、相对原子质量)、粒子结构示意图的含义是正确解答本题的关键.

练习册系列答案
相关题目
19.下列实验操作、现象与解释对应关系正确的是( )
| 实验操作 | 现象或数据 | 结论 | |
| A. | 向收集满 CO2 的软塑料瓶中加入约 $\frac{1}{3}$ 体积的 NaOH 溶液,旋紧瓶盖,振荡 | 塑料瓶变瘪 | CO2 能与NaOH 反应 |
| B. | 20℃时,将 20gKCl 固体加入 50g 蒸馏水中,充分搅拌溶解后,过滤取滤渣并烘干 | 得到 3g 白色固体 | 20℃时,KCl 的溶解度为 34g |
| C. | 向 20mL 白醋中逐滴加入 10mL 氢氧化钠溶液 | 无明显现象 | 白醋与氢氧化钠不反应 |
| D. | 点燃从导管放出的某气体,在火焰上方罩一个冷而干燥的烧杯 | 烧杯内壁有无色液滴产生 | 该气体是 CH4 |
| A. | A | B. | B | C. | C | D. | D |
17.下列实验方案中,能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去氢氧化钠溶液中的碳酸钠 | 加入过量氢氧化钙溶液,过滤 |
| B | 分离铁粉与铜粉 | 用磁铁吸引 |
| C | 除去硫酸钾溶液中的KOH | 加入适量的稀盐酸 |
| D | 鉴别氯化钠溶液、氢氧化钙溶液和稀盐酸 | 滴加无色酚酞溶液,观察颜色的变化 |
| A. | A | B. | B | C. | C | D. | D |
4.下列固体溶于适量水后,液体温度明显升高的是( )
①氢氧化钠②氯化钠③硝酸铵④生石灰.
①氢氧化钠②氯化钠③硝酸铵④生石灰.
| A. | ②④ | B. | ①②③④ | C. | ①④ | D. | ①③④ |
1.化肥为保证粮食丰产起了重要作用.下列化肥属于磷肥的是( )
| A. | 碳酸氢铵(NH4HCO3) | B. | 硫酸钾(K2SO4) | ||
| C. | 硝酸钾(KNO3) | D. | 磷酸二氢钙[Ca(H2PO4)2] |
14.利用如图所示装置,不能完成实验室制取气体的是( )
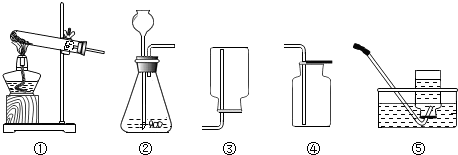

| A. | 用②④制取二氧化碳 | B. | 用②③制取氧气 | ||
| C. | 用②③制取氢气 | D. | 用①⑤制取氧气 |
 哈大齐(哈尔滨-大庆-齐齐哈尔)高铁,是国家“十二五”规划的重点工程.已于2014年10月1日成功试运行,今年上半年正式通车,预计每小时通车一次.哈大齐高铁通车后将与既有的滨州铁路实行客货分运的运输方式,缓解了滨州铁路多年来的运输压力.下列有关说法正确的是( )
哈大齐(哈尔滨-大庆-齐齐哈尔)高铁,是国家“十二五”规划的重点工程.已于2014年10月1日成功试运行,今年上半年正式通车,预计每小时通车一次.哈大齐高铁通车后将与既有的滨州铁路实行客货分运的运输方式,缓解了滨州铁路多年来的运输压力.下列有关说法正确的是( )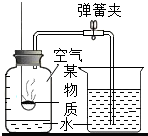 请写出符合下列条件的化学方程式各一个:
请写出符合下列条件的化学方程式各一个: