题目内容
4.物质A与B作用时,只生成物质C与D.6.4g物质A与9.6g物质B恰好完全作用,生成8.8g物质C与7.2g物质D.若物质A、B、C、D的相对分子质量之比为16:16:22:9,则该反应的化学方程式(必须配平)为2A+3B=2C+4D.分析 根据“物质A与B作用时,只生成物质C与D”,则推测A+B=C+D,利用质量守恒定律,推测物质B的质量;根据“物质A、B、C、D的相对分子质量之比为16:16:22:9”,然后利用质量守恒定律可以推测反应的化学方程式的计量数,进行分析解答.
解答 解:
根据“物质A与B作用时,只生成物质C与D”,可以设各物质的计量数分别为abcd,则化学方程式表示为aA+bB=cC+dD,利用质量守恒定律,推测物质B的质量为8.8g+7.2g-6.4g=9.6g;根据“物质A、B、C、D的相对分子质量之比为16:16:22:9”,则设物质A、B、C、D的相对分子质量分别为16、16、22、9.
aA+bB=cC+dD
16a 16b 22c 9d
6.4g 9.6g 8.8g 7.2g
则a:b:c:d等于各自的质量比上各自的相对分子质量,即$\frac{6.4g}{16}:\frac{9.6g}{16}:\frac{8.8g}{22}:\frac{7.2g}{9}$,解得最简计量数为整数:a:b:c:d=2:3:2:4.
则该反应的化学方程式为2A+3B=2C+4D.
故答案为:
9.6;2A+3B=2C+4D
点评 根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和是解题的关键.

练习册系列答案
相关题目
15.下列叙述中,不正确的是( )
| A. | 检验物质中是否含有碳酸根离子时,加入稀盐酸有气泡产生并将气体通入澄清石灰水 | |
| B. | 碳酸钠广泛用于玻璃、造纸、纺织和洗涤剂的生产 | |
| C. | 氢氧化钠俗称烧碱、火碱、苛性钠 | |
| D. | 生成盐和水的反应都是中和反应 |
5.将t℃时硝酸钾饱和溶液降温到T℃,下列有关说法正确的是( )
| A. | 饱和溶液变为不饱和溶液 | |
| B. | 溶液中析出晶体后仍为饱和溶液 | |
| C. | 溶液中析出晶体后变为不饱和溶液 | |
| D. | 溶液中不析出晶体,但仍为饱和溶液 |
6.化学实验时学生获得知识,形成能力的重要方法,下列实验操作方法合理的是( )
| A. | 干燥的药品可以直接放在托盘天平上称量质量 | |
| B. | 向容器中装药品时,应先装液体药品,再装固体药品 | |
| C. | 加热烧杯、试管中的液体时,需用酒精灯隔着石棉网加热 | |
| D. | 收集有氧气的集气瓶,应盖着毛玻璃片,正放在实验桌上 |
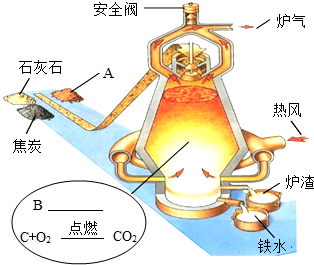 如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁.
如图是炼铁高炉示意图,请写出物质A的名称铁矿石,B处的反应方程式为CO2+C$\frac{\underline{\;高温\;}}{\;}$2CO,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;该高炉中最终的产品为生铁. 由如图中硝酸钾和氯化钠两种物质的溶解度曲线回答:
由如图中硝酸钾和氯化钠两种物质的溶解度曲线回答: