题目内容
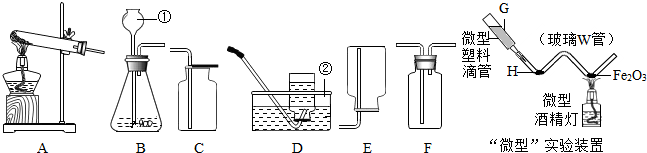
性质决定用途,用途反映性质.工业上常用CO与赤铁矿的主要成分Fe2O3反应炼铁.此反应的化学方程为 ,该反应体现了CO具有 性;Fe2O3中铁元素的化合价为 ,氧元素的质量分数为 .
考点:铁的冶炼,有关元素化合价的计算,元素的质量分数计算,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:根据一氧化碳具有还原性可以还原氧化铁生成铁和二氧化碳以及化合物中各元素的化合价的代数和为0进行解答.
解答:解:一氧化碳具有还原性,一氧化碳可以还原氧化铁生成铁和二氧化碳,化学方程为:3CO+Fe2O3
3CO2+2Fe;化合物中各元素的化合价的代数和为0,Fe2O3中氧元素的化合价为-2价,故铁元素的化合价为+3价.氧元素的质量分数=
×100%=30%.
故答案为:Fe2O3+3CO
2Fe+3CO2;还原;+3;30%.
| ||
| 16×3 |
| 16×3+56×2 |
故答案为:Fe2O3+3CO
| ||
点评:本题难度不大,考查同学们书写化学方程式以及结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
两种化合物都有甜味,下列推测正确的是( )
| A、组成元素一定相同 |
| B、构成分子的原子个数一定相同 |
| C、分子中某些原子的结合方式可能是相似的 |
| D、性质、组成和结构完全相同 |

 如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,成员甲从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.他们依据所学的知识,对此展开探究:
如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂.为了确定盐酸与氢氧化钠是否恰好完全反应,成员甲从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色.他们依据所学的知识,对此展开探究: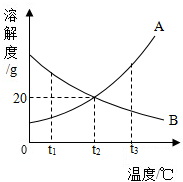 A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题:
A、B两物质的溶解度曲线如图所示,请根据曲线回答下列问题: