题目内容
18.实验室常用的干燥剂“碱石灰”是CaO和固体NaOH的混合物,极易与空气中水蒸汽和CO2反应而变质.某同学对一瓶久置的“碱石灰”作了如下探究:(1)【猜想】
猜想Ⅰ:没有变质,“碱石灰”只含有CaO、固体NaOH;
猜想Ⅱ:已完全变质,“碱石灰”全部变成了CaCO3和Na2CO3.
…
(2)【实验】如图所示
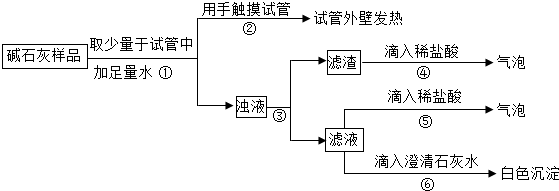
(3)【分析判断】
a.若已知Ca(OH)2、CaCO3和Na2CO3投入到水中不会放热.
b.由操作⑤⑥的现象判断:滤液中含有Na2CO3(写化学式);
c.综合a和b的分析,判断该样品变质情况为部分变质.
(4)【拓展】由上述实验说明,实验室中“碱石灰”应密封保存;操作③中玻棒的作用是引流.
分析 于氧化钙能够和空气中的水发生化学反应生成氢氧化钙,而氢氧化钙和氢氧化钠又容易和二氧化碳反应生成碳酸钙和碳酸钠,因此碱石灰就容易变质.由操作②中的现象不难得出样品中应该还含有氧化钙或固体氢氧化钠,因为氧化钙或固体氢氧化钠遇水会放热,因此猜想II不成立.根据⑤⑥的现象不难得出滤液中应含有碳酸钠,故猜想I不成立,据此分析解答即可;
解答 解:(3)【分析判断】b.向滤渣中加入稀盐酸产生气体,可以知道该滤渣中含有碳酸钙,其方程式为:CaCO3+2HCl=CaCl2+CO2↑+H2O,向滤液中加入稀盐酸和氢氧化钙后产生了气体和沉淀,可以判断在滤液中含有碳酸钠,这说明在固体中有碳酸钙和碳酸钠,所以猜想Ⅰ不成立;
c.结合实验,可以知道在固体中含有碳酸钙,碳酸钠和氧化钙或者氢氧化钠,故可以判断干燥剂是部分变质;
【拓展】在过滤时玻璃棒的作用就是引流,防止溶液外溅.
故答案为:(3)【分析判断】b.Na2CO3;
c.部分变质;
【拓展】引流.
点评 熟练掌握碳酸钠、碳酸钙等碳酸盐和氢氧化钠、氧化钙的化学性质,并能根据所给的实验或者自己设计实验来验证它们是否变质是解题的关键.

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
8.如图是某反应的微观示意图,下列说法正确的是( )


| A. | 该反应生成物中有单质 | |
| B. | 该反应属于化合反应 | |
| C. | 反应前后分子数目没有发生改变 | |
| D. | 反应前甲、乙两种分子的个数比是1:2 |
13.下列是家庭常用清洗剂的pH,呈现酸性的是( )
| A. | 洁厕灵pH=1 | B. | 洗发精pH=8 | C. | 洗衣液pH=10 | D. | 厨房清洁剂pH=13 |
3.对下列问题和事实的解释合理的是( )
| 选项 | 问题和事实 | 解释 |
| A | 电解水生成氢气和氧气 | 水由氢分子和氧分子组成 |
| B | 施肥时氯化铵和熟石灰不能混合施用 | 氯化铵和熟石灰反应生成氨气,降低肥效 |
| C | 可用水润湿的pH试纸测雨水的酸碱度 | 雨水也会湿润pH试纸,故无影响 |
| D | 硫在氧气中燃烧时,集气瓶中先加少量水 | 以防止集气瓶炸裂 |
| A. | A | B. | B | C. | C | D. | D |
1.某同学向过氧化氢溶液中加入二氧化锰制取氧气,相关数据如表:
请计算:
(1)该同学制得氧气的质量为1.6g.
(2)该同学所用过氧化氢溶液的溶质质量分数.(相对原子质量:H-1 O-16)
| 反应前物质的质量/g | 充分反应后物质的质量/g |
| 过氧化氢溶液+二氧化锰 | 固体与液体混合物质量 |
| 68.0+0.1 | 66.5 |
(1)该同学制得氧气的质量为1.6g.
(2)该同学所用过氧化氢溶液的溶质质量分数.(相对原子质量:H-1 O-16)
18.下列物质的分类正确的是( )
| A. | 合金:生铁、赤铜、青铜 | |
| B. | 有机物:甲烷、酒精、葡萄糖 | |
| C. | 纯净物:冰水混合物、纯碱、98%浓硫酸 | |
| D. | 氧化物:双氧水、生石灰、烧碱 |
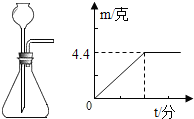 小明用如图发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.
小明用如图发生装置来制取二氧化碳,老师给他提供了石灰石、无标签的稀盐酸和氯化钠水溶液各一瓶.