题目内容
20.蛋白质是人体必需的营养物质,它在人体内最终分解为( )| A. | 葡萄糖 | B. | 维生素 | C. | 脂肪酸 | D. | 氨基酸 |
分析 根据蛋白质水解生成氨基酸进行分析.
解答 解:蛋白质是由氨基酸组成,它水解的最终产物是氨基酸.
故选D.
点评 本题注意化学与生活的联系,涉及营养素和蛋白质的性质等基础知识,题目难度不大,注意积累化学知识即可解答.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.下列有关金属及合金的说法中正确的是( )
| A. | “真金不怕火炼”说明黄金的硬度非常大 | |
| B. | 金属活动性顺序表中,银前面的金属都能置换出AgCl中的银 | |
| C. | 合金是由两种或两种以上金属熔合而成的具有金属特性的物质 | |
| D. | 在日常生活中,大量使用的常常不是纯金属,而是它们的合金 |
15.下列物质中,属于纯净物的是( )
| A. | 蔗糖 | B. | 黄酒 | C. | 白醋 | D. | 酱油 |
9.下列实验操作正确的是( )
| A. | 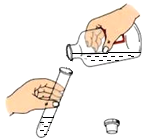 倾倒液体 | B. | 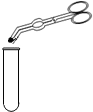 加入块状固体 | C. | 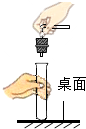 塞紧橡皮塞 | D. | 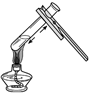 加热液体 |
19.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3(化学式);
猜想3:该漂白粉全部变质,固体成分为CaCl2和CaCO3.
【实验探究】限选试剂:盐酸、澄清的石灰水、品红溶液.
【交流与反思】
(1)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的酸性会增强(选填“增强”、“减弱”或“不变”).
(2)写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3(化学式);
猜想3:该漂白粉全部变质,固体成分为CaCl2和CaCO3.
【实验探究】限选试剂:盐酸、澄清的石灰水、品红溶液.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量盐酸,塞上带导管的单孔塞 把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2 成立 |
| ②在上述反应后的试管 中加少量品红溶液. | 品红溶液褪色. |
(1)HClO在常温下分解,反应为2HClO═2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的酸性会增强(选填“增强”、“减弱”或“不变”).
(2)写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2 +2HCl=2HClO+CaCl2.
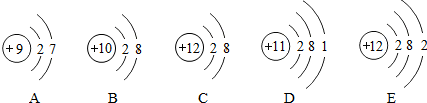
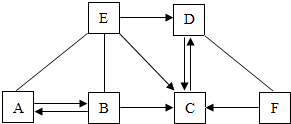 已知A、B、C、D、E分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂.F是常见的一种红棕色物质,它们之间存在如图所示的关系(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题:
已知A、B、C、D、E分别是初中化学常见的五种不同类别的物质,其中B的固体和E的浓溶液常用作实验室的干燥剂.F是常见的一种红棕色物质,它们之间存在如图所示的关系(图中“-”表示两端的物质能反应,“→”表示物质间存在转化关系,部分物质和反应条件未标出).请按要求回答下列问题: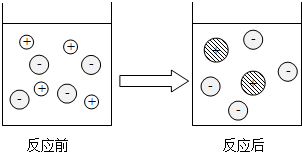 在宏观、微观、符号之间建立联系是化学特有的思维方式.在稀盐酸中加入过量锌粒制取氢气的实验中:
在宏观、微观、符号之间建立联系是化学特有的思维方式.在稀盐酸中加入过量锌粒制取氢气的实验中: ①
① ③
③ ②
②