题目内容
四氧化三铁可用于医疗器械、电子等工业。某工厂采利用工业废液(含FeSO4和少量
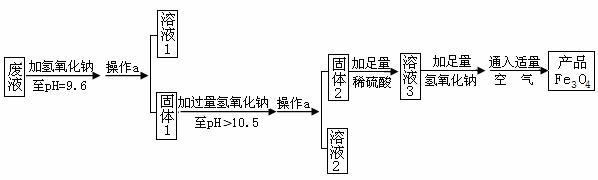 ZnSO4、MgSO4),进行四氧化三铁的制备流
ZnSO4、MgSO4),进行四氧化三铁的制备流 程如下:
程如下:
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH 范围如表所示 。
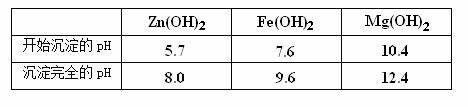
(2)25℃时,Zn(OH)2可溶于pH >10.5 的碱溶液。
【回答问题】
(1)往废液中加入氢氧化钠溶液 生成沉淀的化学方程式为:
生成沉淀的化学方程式为:
▲ (任写一个)。
(2)操作a 的名称为 ▲ 。该操作需要的玻璃仪器有烧杯、玻璃棒、 ▲ 等。
(3)溶液1 所含溶质有 ▲ 。(任写两种)
(4)若用废液1000kg,最终得到产品四氧化三铁质量为23.2kg,则原废液中硫酸亚铁溶质的质量分数不低于 ▲ (精确到0.01% )。
(1) FeSO4+2NaOH=Fe(OH) 2↓+Na2SO4 或ZnSO4 + 2NaOH = Zn(OH) 2↓+ Na2SO4
(2) 过滤 漏斗
(3) Na2SO4 、MgSO4、NaOH (任填2种)
(4) 4.56%

下表各物质都含有少量杂质,分别写出除去杂质应选用的物质及所发生的化学反应方式程式。
| 物质 | 杂质 | 除杂质选用的物质 | 发生反应的化学方程式 |
| 稀盐酸 | 稀H2SO4 | ||
| CO | CO2 | ||
| NaCl | Na2CO3 |
 :①⑥⑦⑧
:①⑥⑦⑧ 表示向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
表示向一定体积的稀盐酸中逐滴加入氢氧化钠溶液
 的质量变化,测算氧化铁样品中含有Fe2O3的质量分数。试验中,在其他操作正常的条件下,若下列情况出现,请你对测算出的结果与实际值相比较,并作出判断(用“偏小”“偏大”“不受影响”之一填写下列空白)。
的质量变化,测算氧化铁样品中含有Fe2O3的质量分数。试验中,在其他操作正常的条件下,若下列情况出现,请你对测算出的结果与实际值相比较,并作出判断(用“偏小”“偏大”“不受影响”之一填写下列空白)。