题目内容
4.实验室一般不用块状石灰石与稀硫酸反应制取二氧化碳,原因是碳酸钙与硫酸反应生成的硫酸钙微溶,覆盖在石灰石的表面阻止与硫酸充分接触而终止反应.小明查阅资料后发现,在石灰石与硫酸反应停止后,加入少量氯化钠固体,能使反应继续进行,而加入少量的硝酸钾或硫酸铵固体却没现象.氯化钠中哪种成分促使石灰石与硫酸持续反应呢?小明设计了如下实验:向5支试管里各加入一块大小相近的石灰石和5毫升溶质质量分数为50%的硫酸,待反应停止后,再分别加入约0.2克的NaCI、KCl、NH4Cl、NaNO3、Na2SO4固体轻轻振荡.观察到的现象记录于表:| 实验组次 | 1 | 2 | 3 | 4 | 5 |
| 物质 | NaCl | KCl | NH4Cl | NaNO3 | Na2SO4 |
| 现象 | 继续发生反应生成气体,速度较快 | 继续反应生成气体,速度较慢 | 继续反应生成气体,速度较慢 | 没有很明显可见的现象 | 没有很明显可见的现象 |
(2)小明为了研究Na+在实验中的作用,你认为应选择哪几组实验进行观察?1、2、3.
(3)通过实验可得出的结论是加快石灰石与硫酸反应是Na+与Cl-共同起作用;Cl-所起的用比Na+大.
分析 (1)判断反应快慢的方法是:比较相同时间内产物生成多少或生成同量的产物所需时间的多少.
(2)根据条件选择含有钠离子的溶液分析;
(3)根据实验现象结合探究目的得出结论.
解答 解:(1)判断反应快慢的方法可以是:比较相同时间内产生气泡的多少,
(2)为了验证Na+在实验中的作用,要以Na+作为实验的唯一变量;所以可以选择1、2、3组实验进行观察;
(3)根据表格现象可知:加快石灰石与硫酸反应是Na+与Cl-共同起作用,Cl-所起的用比Na+大,钙离子对该反应起抑制作用;或加快石灰石与硫酸反应是Na+与Cl-共同起作用,Cl-所起的用比Na+大;或加快石灰石与硫酸反应是Na+与Cl-共同起作用,钙离子对该反应起抑制作用(只答加快石灰石与硫酸反应是Na+与Cl-共同起作用即可);
故答案为:(1)比较相同时间内产生气泡的多少;
(2)1、2、3;
(3)加快石灰石与硫酸反应是Na+与Cl-共同起作用(或Na+与Cl-对加快石灰石
与硫酸反应都起作用);Cl-所起的用比Na+大.
点评 本题属于信息题的考查,难度较大,可以依据题目的信息结合实验的目的进行分析,能够考查学生的分析问题能力、解决问题能力.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
9.水是化学实验中常见且用途广泛的一种物质.对下列各实验中水的主要作用的解释不合理的是( )
| A. | 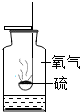 硫在氧气中燃烧--集气瓶好做水:吸收放出的热量 | |
| B. | 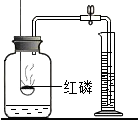 测定空气中氧气含量--量筒中的水:通过水体积变化得到氧气体积 | |
| C. |  细铁丝在氧气中燃烧--集气瓶中的水:防止集气瓶炸裂 | |
| D. | 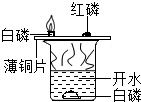 探究燃烧的条件--烧杯中的水:加热铜片:隔绝空气 |
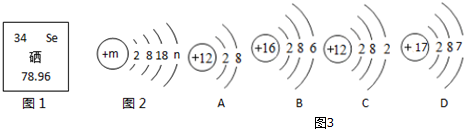
 有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.
有A、B、C、D四种物质,如图所示,A、B、C在一定下可以发生转化,在C溶液中通入CO2,溶液变浑浊,生成白色沉淀A.D与A、B、C均能发生反应,D与C发生中和反应,D与A反应有CO2气体产生,D与AgNO3溶液反应,可产生不溶于稀硝酸的白色沉淀.