题目内容
6.石灰厂为了测定一批石灰石样品中碳酸钙的质量分数,取用4g石灰石样品,把20g稀盐酸分4次加入样品中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如表:| 实验次数 | 第一次 | 第二次 | 第三次 | 第四次 |
| 稀盐酸的用量 | 5g | 5g | 5g | 5g |
| 剩余固体的质量 | 3g | 2g | 1g | 1g |
(2)计算该稀盐酸的溶质质量分数(写出计算过程,结果精确到0.1%).
(3)第三次加入5g稀盐酸后所得溶液的质量为16.68g.
分析 (1)由于样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶于水,因此第三次、第四次实验所剩余的固体即不发生反应也不溶于水的杂质固体的质量;
(2)根据反应的化学方程式,由参加反应的碳酸钙的质量计算盐酸完全反应时消耗的HCl的质量,计算该稀盐酸的质量分数;根据实验数据,前三次所加入的稀盐酸都完全发生了反应,在计算稀盐酸的溶质质量分数时可使用前三次的实验数据.
(3)根据质量守恒定律来分析解答;
解答 解:(1)每加入5g稀盐酸可反应1g碳酸钙,而第四次加入稀盐酸所剩余固体质量却没减少,说明碳酸钙已完全反应,剩余固体为杂质;则
石灰石样品中碳酸钙的质量分数=$\frac{4g-1g}{4g}×100%$=75%
故答案为:75%;
(2)由表中数据可知第三次加入5g稀盐酸后,3g碳酸钙与15g稀盐酸刚好完全反应.
设稀盐酸中溶质的质量为x.
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
3g x y
$\frac{100}{3g}=\frac{73}{x}$
x=2.19g
稀盐酸中溶质的质量分数=$\frac{2.19g}{15g}$×100%=14.6%
答:稀盐酸中溶质的质量分数为14.6%.
(3)$\frac{100}{3g}=\frac{44}{y}$
y=1.32g
第三次加入5g稀盐酸后所得溶液的质量为:3g+15g-1.32g=16.68g;
答案:16.68g.
点评 根据反应进行参加反应的溶液溶质质量分数计算时,一定要选取溶液中溶质完全反应时的数据计算溶液中溶质的质量,这样求得的溶质质量才是溶液中全部溶质的质量.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
16. 牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
探究一:牙膏的酸碱性
实验1:取少量牙膏放入烧杯中,加入足量的水溶解,静置,取上层清液,测定溶液的 pH,pH>7(填”>”或”<”),牙膏呈碱性.
探究二:牙膏摩擦剂的成分
小明同学发现实验1烧杯底部有沉淀,便想探究其成分.
【查阅资料】牙膏成分中的固体原料为磨擦剂,它是擦去牙齿表面牙垢,减轻牙渍的成分.常见的摩擦剂有碳酸钙、二氧化硅(SiO2)等.
【猜想与假设】该牙膏摩擦剂成分可能是:①为碳酸钙;②二氧化硅;③你的猜想是碳酸钙和二氧化硅混合物.
实验2:【设计方案和实验】
请你写出步骤①的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
 牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:
牙膏是和牙刷一起用于清洁牙齿,保护口腔卫生,是对人体安全的一种日用必需品.某化学兴趣小组对某种牙膏的成分进行了如下探究:探究一:牙膏的酸碱性
实验1:取少量牙膏放入烧杯中,加入足量的水溶解,静置,取上层清液,测定溶液的 pH,pH>7(填”>”或”<”),牙膏呈碱性.
探究二:牙膏摩擦剂的成分
小明同学发现实验1烧杯底部有沉淀,便想探究其成分.
【查阅资料】牙膏成分中的固体原料为磨擦剂,它是擦去牙齿表面牙垢,减轻牙渍的成分.常见的摩擦剂有碳酸钙、二氧化硅(SiO2)等.
【猜想与假设】该牙膏摩擦剂成分可能是:①为碳酸钙;②二氧化硅;③你的猜想是碳酸钙和二氧化硅混合物.
实验2:【设计方案和实验】
| 步骤 | 现象 | 结论 |
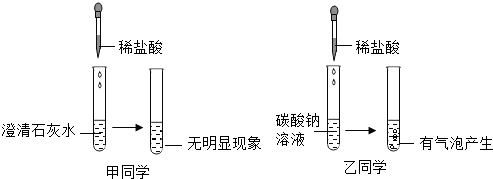
| ①取少量沉淀,加入适量稀盐酸 | 沉淀完全溶解,有气泡产生 | 假设①正确(填序号) |
| ②将产生的气体通入澄清的石灰水 | 澄清石灰水变浑浊 |
14.生活中的下列物品加入适量水后,可以形成溶液的是( )
| A. | 冰块 | B. | 蔗糖 | C. | 面粉 | D. | 奶油 |
18.在一密闭容量内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化如图,下列说法正确的是( )


| A. | 该反应为化合反应 | B. | 丙一定没有参加反应 | ||
| C. | 反应中甲、乙改变的质量比为1:3 | D. | 丁相对分子质量是甲的2倍 |

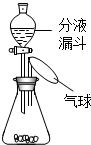 某化学兴趣小组设计了一组“吹气球”实验,装置如图所示.要求用四种不同反应类型的反应使装置中的气球涨大,请写出各反应类型中分液漏斗和锥形瓶中的试剂组合.
某化学兴趣小组设计了一组“吹气球”实验,装置如图所示.要求用四种不同反应类型的反应使装置中的气球涨大,请写出各反应类型中分液漏斗和锥形瓶中的试剂组合.