题目内容
10.下列计算过程和结果都正确的是( )| A. | 在t℃时,将35gKCl溶液蒸干得到7gKCl固体,则在t℃时原溶液的溶质质量分数为$\frac{7g}{35g-7g}$×100%=25% | |
| B. | 将30%的100g硫酸溶液稀释至其溶质质量分数为15%,设需加水的质量为X,则100g×30%=X×15%,X=200g | |
| C. | 在t℃时,把100g10%的食盐水中蒸发50g水后,所得新的食盐溶液溶质质量分数为$\frac{100g×10%}{100g-50g}$×100%=20% | |
| D. | 将40g15%的硝酸钠溶液跟60g30%的硝酸钠溶液混合,则可得溶液质质量分数为:$\frac{40g×15%+60g×30%}{40g+60g}$×100%=24% |
分析 根据已有的溶液计算进行分析解答,加水稀释前后溶质质量不变,在计算时一定分清溶液中溶质、溶剂和溶液的质量.
解答 解:A、在某温度下,将35g KCl溶液蒸干得到7gKCl固体,则原溶液溶质质量分数为$\frac{7g}{35g}$×100%=20%,错误;
B、将30%的100g硫酸溶液稀释至其溶质质量分数为15%,设需加水的质量为X,则100g×30%=(100g+X)×15%,X=100g,错误;
C、在t℃时,把100g10%的食盐水中蒸发50g水后,所得新的食盐溶液溶质质量分数为$\frac{100g×10%}{100g-50g}$×100%=20,正确;
D、将40g15%的硝酸钠溶液跟60g30%的硝酸钠溶液混合,则可得溶液质质量分数为:$\frac{40g×15%+60g×30%}{40g+60g}$×100%=24%.正确.
故选CD.
点评 本题考查了根据溶液的有关计算,完成此题,可以依据已有的知识进行.

练习册系列答案
相关题目
18.下列变化中,属于物理变化的是( )
| A. |  铁生锈 | B. |  水灌溉农田 | ||
| C. |  酸雨浸蚀大理石雕像 | D. |  动植物呼吸 |
5.推理是学习化学的一种方法,以下推理正确的是( )
| A. | 氧化物一定含氧元素,则含氧元素的化合物一定是氧化物 | |
| B. | 含CO32-的物质与盐酸反应会产生气体,但与盐酸反应生成气体的物质不一定都含有CO32- | |
| C. | 溶液一定是均一稳定的物质,则均一稳定的物质一定是溶液 | |
| D. | 同种分子构成的物质一定是纯净物,则纯净物一定都是由同种分子构成的 |
2.一定条件下.下列物质在密闭容器内充分反应,测得反应前后各物质的质量如表:
则反应后x的值为39.4 g;该反应中B和D两种物质变化的质量比为87:32.
| 物质 | A | B | C | I) |
| 反应前质量/g | 19.7 | 8.7 | 31.6 | 0.4 |
| 反应后质量/g | x | 17.4 | 0 | 3.6 |
19.下列四个图象能正确反映其对应实验操作的是( )
| A. | 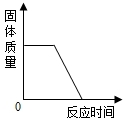 高温煅烧一定质量的石灰石 高温煅烧一定质量的石灰石 | |
| B. | 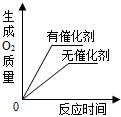 用等质量、等浓度的双氧水分别制取氧气 用等质量、等浓度的双氧水分别制取氧气 | |
| C. | 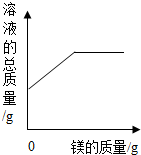 向一定质量的硫酸溶液中逐渐加入镁条至过量 向一定质量的硫酸溶液中逐渐加入镁条至过量 | |
| D. | 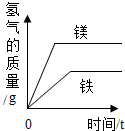 等质量的镁、铁分别与足量的相同的稀盐酸反应 等质量的镁、铁分别与足量的相同的稀盐酸反应 |
20.区别二氧化碳、氧气和空气三种气体,应采用的方法是( )
| A. | 将气体分别通入澄清的石灰水中 | B. | 将燃着的木条分别伸入集气瓶中 | ||
| C. | 将气体分别通入水中 | D. | 观察三种气体的颜色 |
 下列仪器是化学实验中常用的仪器.
下列仪器是化学实验中常用的仪器.