题目内容
9.某同学用一定量 Cu(NO3)2和 Zn(NO3)2的混合溶液进行了如图实验.则对溶液甲和固体乙成分的描述正确的是( )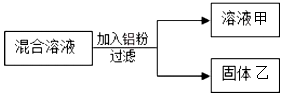
| A. | 溶液甲中一定有 Zn(NO3)2和 Al(NO3)3 | |
| B. | 溶液甲中一定有 Cu(NO3)2和 Al(NO3)3 | |
| C. | 固体乙中一定有 Cu,可能有 Zn和 Al | |
| D. | 固体乙中一定有 Cu和 Zn,可能有 Al |
分析 根据金属活动性顺序及其运用分析,排在氢之前的金属可与稀盐酸或稀硫酸反应产生氢气,排在前面的金属(除钾、钙、钠外)可将排在后面的金属从其盐溶液中置换出来,Zn(NO3)2和Cu(NO3)2都会与铝粉反应.
解答 解:由于金属的活动顺序是:铝>锌>铜,向一定量 Cu(NO3)2和 Zn(NO3)2的混合溶液加入铝粉,铝先与硝酸铜反应生成了硝酸铝和铜,当硝酸铜完全反应后,铝再与硝酸锌反应生成了硝酸铝和锌.由此可知:
A、如果铝粉过量,溶液甲中一定只含有硝酸铝,一定不含硝酸锌,故A错误;
B、如果铝粉过量,溶液甲中一定含有硝酸铝,一定不含硝酸铜,故B错误;
C、无论铝粉的质量是多少,滤渣中一定有铜,Zn和 Al是可能含有的,故C正确;
D、如果铝粉的量很少,则只能置换出铜,因此,固体乙中一定含有铜,可能有锌和铝,故D错误.
故选:C.
点评 本题难度不是很大,主要考查了对金属活动性顺序的应用和理解,培养学生的应用能力和解决问题的能力.

练习册系列答案
相关题目
17.加碘食盐就是在食盐(主要成分NaCl)中添加碘酸钾(化学式KIO3),下列有关说法正确的是( )
| A. | NaCl是由分子构成的 | B. | KIO3中碘元素的化合价为+5 | ||
| C. | KIO3中含量最多的元素是氧元素 | D. | 加碘食盐属于盐类 |
4.下列实验操作正确的是( )
| A. | 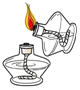 点燃酒精灯 | B. |  闻气味 | C. | 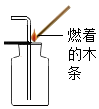 二氧化碳验满 | D. | 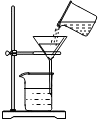 过滤 |
14.除去下列物质中的少量杂质,所用试剂或方法不正确的是( )
| 选项 | 物质 | 所含杂质 | 试剂或方法 |
| A | N2 | O2 | 通过足量灼热的铜丝 |
| B | CO2 | HCl | 通过饱和碳酸氢钠溶液 |
| C | MnO2 | KCl | 加足量水,过滤 |
| D | CO | H2O和CO2 | 先通过浓硫酸,再通过氢氧化钠溶液 |
| A. | A | B. | B | C. | C | D. | D |
1.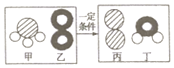 甲和乙在一定条件下反应生成丙和丁,微观示意图如图所示,不同圆球代表不同原子,下列说法错误的是( )
甲和乙在一定条件下反应生成丙和丁,微观示意图如图所示,不同圆球代表不同原子,下列说法错误的是( )
 甲和乙在一定条件下反应生成丙和丁,微观示意图如图所示,不同圆球代表不同原子,下列说法错误的是( )
甲和乙在一定条件下反应生成丙和丁,微观示意图如图所示,不同圆球代表不同原子,下列说法错误的是( )| A. | 该反应前后一共有三种原子 | |
| B. | 该反应属于置换反应 | |
| C. | 该反应前后一定有元素化合价发生改变 | |
| D. | 该反应前后分子个数没有改变 |
19.近日有媒体报道,我国科学家发现“把二氧化碳变成汽油”的高效转化新途径.即通过设计一种新型多功能复合催化剂,首次实现了CO2直接加氢制取汽油.被同行誉为“CO2催化转化领域的突破性进展”,据此,你认为下列说法不正确的是( )
| A. | 新途径可有效缓解全球温室效应 | B. | 此技术可减少对化石燃料的依赖 | ||
| C. | 该转化过程中没有发生化学变化 | D. | 催化剂对转化起着举足轻重作用 |