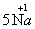题目内容
(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象.
(2)将一定量的锌粉放入稀盐酸、氯化亚铁、氯化铜的混合溶液中,充分反应后过滤,再向滤渣中加盐酸有气泡产生.则滤渣中一定含有的固体是 ;滤液中一定不含的物质是 .
解:(1)铁锈的主要成分是氧化铁(Fe2O3),将生锈的铁钉放入稀盐酸中,先是表面的铁锈的主要成分氧化铁与盐酸反应生成氯化铁与水,反应的化学方程式为:Fe2O3+6HCl═2FeCl3+3H2O;当铁锈完全反应后,铁与过量的稀盐酸发生反应,生成氯化亚铁与氢气,会观察到有气泡冒出.
(2)由金属活动性顺序表可知,金属的活动性是:锌>铁>氢>铜.将一定量的锌粉放入稀盐酸、氯化亚铁、氯化铜的混合溶液中,锌首先与氯化铜反应生成铜和氯化锌,当氯化铜反应完成后,锌再与稀盐酸反应生成氯化锌和氢气,然后与氯化亚铁反应生成铁和氯化锌,在滤出的固体中滴加稀盐酸,有气泡产生,说明固体中含有的金属中有能与盐酸反应的金属,该金属可能是铁或锌,由题意,不能确定锌是否有剩余,故滤渣中一定含有的固体是铜和铁;溶液中的氯化铜、盐酸已经被锌完全反应,则滤液中一定不含的物质是HCl和CuCl2.
故答案为:(1)Fe2O3+6HCl=2FeCl3+3H2O;有气泡冒出;(2)Fe和Cu;HCl和CuCl2

(1)用化学符号表示:
①地壳在含量最多的金属元素 ;
②氧化镁中阳离子 .
(2)化学与人类的生产、生活密切相关.
①铁锅常用于炒饭炒菜,是利用了铁的 性;
②化学电池是将化学能直接转化为 的装置.
根据金属活动性顺序Fe>Cu>Ag判断,下列说法错误的是( )
|
| A. | 反应Cu+FeSO4═Fe+CuSO4可以发生 |
|
| B. | 反应Fe+2AgNO3═2Ag+Fe(NO3)2可以发生 |
|
| C. | 铜片放入硝酸银溶液中,颜色由无色变成蓝色 |
|
| D. | 铁丝插入硫酸铜溶液中,铁丝表面有红色物质析出 |
根据表中的数据,回答下列问题。
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | NaC | 35. 7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
(1)40℃时,NaCl的溶解度是 。
(2) 20℃时,称取31.6g KNO3固体加入盛有100g水的烧杯中,充分溶解形成的溶液是 (填“饱和”或“不饱和”)溶液;称取31.6g KNO3固体时,发现托盘天平指针偏右,接下来的操作是 。
(3)当KNO3中混有少量NaCl时,提纯KNO3所采用的方法是 。
(4)当等质量KNO3的饱和溶液和NaCl的饱和溶液从60℃降温到20℃,对所得溶液的叙述正确的是(填序号) 。
A.都是饱和溶液 B.溶剂质量:KNO3>NaCl C.溶液质量:KNO3<NaCl






 ,再用带火星的木条试验
,再用带火星的木条试验 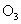
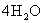 D.5个钠离子—
D.5个钠离子—