题目内容
某补钙品(有效成分为碳酸钙,其他成分不含钙元素)的说明中标明含钙量为25%。质量监督员为了检验该产品,取10 g补钙品放入100 g稀盐酸中,HCl与补钙品的有效成分刚好完全反应(其他成分不与盐酸反应)。反应后剩余固体和液体的总质量比反应前减少了2.2 g。求:
(1)补钙品中实际含钙的质量分数是多少?是否符合标签说明?
(2)所用稀盐酸中溶质的质量分数是多少?
解:(1)设碳酸钙的质量为x,设所用稀盐酸中溶质HCl的质量为y。
CaCO3+2HCl===CaCl2+H2O+CO2↑
100 73 44
x y 2.2 g
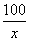 =
=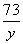 =
=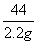
解得x=5 g,y=3.65 g
(1)所以钙元素质量为5 g×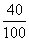 =2 g
=2 g
则钙元素的质量分数=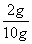 ×100%=20%
×100%=20%
20%小于标签中标明的含量25%,是不符合标签说明的。
(2)所用稀盐酸中HCl质量分数=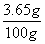 ×100%=3.65%
×100%=3.65%
答:略。

 阅读快车系列答案
阅读快车系列答案元素周期表是化学学习和研究的重要工具,下图是元素周期表的一部分。
| ⅠA | 0 | ||||||||
| 第一周期 | 1 H 氢 1.008 | 2 He 氦 4.003 | |||||||
| ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||||
| 第二周期 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 | |
| 第三周期 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar氩 39.95 |
 (1)某微粒的结构示意图为 ,该微粒是元素周期表中的__ _ _元素,它
(1)某微粒的结构示意图为 ,该微粒是元素周期表中的__ _ _元素,它
的核电荷数是_______,碳元素的核电荷数是_______,由此可知不同元素的本质区别是_______
 ___________________。
___________________。
(2)硫原子的结构示意图为  ,在化学反应中易___________(填“得”或“失”)
,在化学反应中易___________(填“得”或“失”)
电子,是_____________(填“金属”或“非金属”)元素。
 反应后所得溶液中
反应后所得溶液中 原子的原子核都由质子和中子构成
原子的原子核都由质子和中子构成