题目内容
6.A、B、C三种溶液两两混合后的实验现象如图所示,则A、B、C三种溶液依次是( )
| A. | 盐酸、碳酸钠溶液、澄清石灰水 | |
| B. | 氯化钠溶液、澄清石灰水、氢氧化钠溶液 | |
| C. | 盐酸、碳酸钠溶液、氢氧化钠溶液 | |
| D. | 氢氧化钙溶液、盐酸、硫酸钠溶液 |
分析 根据A、B反应会生成气体,B、C反应会生成生成沉淀,A、C反应没有明显现象,然后结合题中的选项进行验证即可.
解答 解:A、盐酸和碳酸钠反应会生成二氧化碳气体,氢氧化钙和碳酸钠反应会生成碳酸钙沉淀,氢氧化钙和盐酸反应生成氯化钙,没有明显现象,符合题意,故A正确;
B、氯化钠和澄清石灰水不会反应,没有明显现象,不符合题意,故B错误;
C、盐酸和碳酸钠反应会生成二氧化碳气体,氢氧化钠和碳酸钠不会反应,没有明显现象,不符合题意,故C错误;
D、氢氧化钙和盐酸反应没有明显现象,不符合题意,故D错误.
故选:A.
点评 本题主要考查了如何根据实验现象判断物质的组成方面的问题,解答类似题目可以从给定的选项直接分析,而不需要从题干去分析,这样可以节省时间,提高准确率.

练习册系列答案
相关题目
16.某物质(仅含一种溶质)的溶液在t℃时,恒温蒸发掉10g水,析出了2g晶体,再恒温蒸发掉10g水,又析出了3g晶体,则下列说法正确的是( )
| A. | 原溶液中t℃时一定是饱和溶液 | |
| B. | t℃时该溶质溶解度为20克 | |
| C. | t℃时该溶质溶解度为30克 | |
| D. | 最后剩余溶液的溶质质量分数比原溶液的溶质质量分数小 |
17.在加入酚酞能够变红的溶液中,下列各组离子一定能大量共存的是( )
| A. | H+、Cl-、Na+ | B. | Ca2+、SO42-、CO32- | ||
| C. | Na+、K+、Cl- | D. | NH4+、NO3-、CO32- |
14. 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
(1)碳酸钠、碳酸氢钠溶液都能使紫色石蕊试液变成蓝色.
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
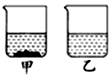
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.
 不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示
不同温度下,碳酸钠和碳酸氢钠的溶解度如表所示| 温度/℃ | 0 | 20 | 40 | 60 |
| 碳酸钠 | 7.0 | 21.8 | 48.8 | 46.4 |
| 碳酸氢钠 | 6.9 | 9.6 | 12.7 | 16.4 |
(2)服用碳酸氢钠治疗胃酸过多时,胃液的pH增大(填“增大”、“减小”或“不变”),发生反应的化学方程式是NaHCO3+HCl=NaCl+H2O+CO2↑.
(3)为区分碳酸钠和碳酸氢钠两种白色固体.在20℃时,各盛有100mL水的甲、乙两烧杯中,分别加入等质量的碳酸钠和碳酸氢钠固体,充分溶解后,现象如图所示.乙烧杯中加入的物质是Na2CO3(填化学式),加入的质量m的范围为:大于9.6g小于等于21.9g.
11.实验室许多药品需要密封保存.下列药品需密封保存的原因,解释错误的是( )
| A. | 浓盐酸--防止挥发 | B. | NaOH固体--防止其潮解和变质 | ||
| C. | 浓硫酸--防止吸水 | D. | 生石灰--防止与氧气反应 |
18.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
| A. | 用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码 | |
| B. | 将配好的氯化钠溶液转移到细口瓶中时,不慎洒出部分溶液 | |
| C. | 用量筒量取蒸馏水读数时,仰视凹液面的最低处 | |
| D. | 将量筒中的水倒入烧杯时,有水洒出 |
15.下列混合物,属于溶液的是( )
| A. | 牛奶 | B. | 肥皂水 | C. | 钡餐液 | D. | 碘酒 |