题目内容
15.(1)氯原子的最外层有7个电子,氯原子在化学反应中比较容易得电子.(2)酸在水中电离时,电离出的阳离子一定是氢离子.盐在水中电离时,电离出的阴离子都叫做酸根离子.实验室制氧气时用的氯酸钾溶解于水中,电离出的阳离子是K+,电离出的阴离子是ClO3-.(用化学式表示)
分析 (1)根据氯原子的最外层电子数目的特点分析回答;
(2)根据酸碱盐的组成、解离出的离子的特点分析回答.
解答 解:(1)氯原子的最外层有7个电子,大于4,氯原子在化学反应中比较容易得电子.
(2)酸在水中电离时,电离出的阳离子一定是氢离子.盐在水中电离时,电离出的阴离子都叫做酸根离子.实验室制氧气时用的氯酸钾溶解于水中,电离出的阳离子是K+,电离出的阴离子是氯酸根离子,符号为:ClO3-.故答为:(1)7,得;(2)氢离子,酸根离子,ClO3-.
点评 本题的难度不大,了解常见原子的结构、酸碱盐的组成特点即可分析解答.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
5.某有机物12.8g在16g氧气中燃烧,得到一氧化碳、二氧化碳、水蒸气的混合气体共28.8g.为测定混合气体中各种气体的质量,甲、乙、丙三位同学设计了下列实验方案(假定每步反应都完全进行,每次都能准确测定装置的质量变化甲方案:将混合气体先通过浓硫酸,再通过用酒精灯加热的氧化铜乙方案:将混合气体先通过浓硫酸,再通过碱石灰(CaO、NaOH)丙方案:将混合气体先通过碱石灰,再通过浓硫酸下列对三种实验方案的评价正确的是( )
| A. | 三种实验方案都能测定混合气体的组成 | |
| B. | 三种实验方案都不能测定混合气体的组成 | |
| C. | 甲乙两种实验方案都能测定混合气体的组成,但甲方案需作改进,添加尾气处理装置 | |
| D. | 甲乙两种实验方案都能测定混合气体的组成,但乙方案需作改进,添加尾气处理装置 |
6.有两杯无色液体,一杯是蒸馏水,另一杯是饱和食盐水,请利用所学过的知识将它们鉴别开来,并在表中简述操作方法和得到的结论.
| 操作方法 | 结论 | |
| 例 | 取少量液体蒸干 | 能留下固体颗粒是饱和食盐水 |
| (1) | ||
| (2) | ||
| (3) |
10. 为了探究中和反应,甲、乙两名同学分别进行以下实验.
为了探究中和反应,甲、乙两名同学分别进行以下实验.
(1)甲同学向装有少量Ca(OH)2溶液的试管中倒入一定量的稀盐酸,然后滴加几滴酚酞试液,发现酚酞不变色,此现象能(填“能”或“不能”)说明盐酸与氢氧化钙发生了反应.
(2)乙同学向滴有酚酞的NaOH溶液中逐滴加入稀盐酸,边滴加边振荡,“振荡”的目的是使药品充分接触,在滴加过程中,乙同学意外发现有气泡产生,通过思考认为该氢氧化钠溶液已变质,变质的原因是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
(3)乙同学为了检验该氢氧化钠溶液的变质程度,设计实验方案并得出结论.
(4)实验结束后,甲、乙两名同学将三支试管中的废液倒入同一洁净烧杯中,得到无色澄清溶液,分析所得溶液中溶质的成分为①CaCl2、NaCl;②CaCl2、NaCl、HCl(其他答案合理即可).
 为了探究中和反应,甲、乙两名同学分别进行以下实验.
为了探究中和反应,甲、乙两名同学分别进行以下实验.(1)甲同学向装有少量Ca(OH)2溶液的试管中倒入一定量的稀盐酸,然后滴加几滴酚酞试液,发现酚酞不变色,此现象能(填“能”或“不能”)说明盐酸与氢氧化钙发生了反应.
(2)乙同学向滴有酚酞的NaOH溶液中逐滴加入稀盐酸,边滴加边振荡,“振荡”的目的是使药品充分接触,在滴加过程中,乙同学意外发现有气泡产生,通过思考认为该氢氧化钠溶液已变质,变质的原因是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示).
(3)乙同学为了检验该氢氧化钠溶液的变质程度,设计实验方案并得出结论.
| 实验操作 | 实验现象 | 实验结论 |
| 取样于试管中,先滴加过量CaCl2溶液[或BaCl2、Ba(NO3)2、Ca(NO3)2], 再滴加酚酞溶液. | 有白色沉淀生成,酚酞溶液变红 | 氢氧化钠溶液 部分变质 |
20.下列状态的物质能导电的是( )
| A. | 液态纯硫酸 | B. | 固态氯化钠 | C. | 熔化的硝酸钾 | D. | 酒精溶液 |
7.下列各组中都有两种物质的名称,它们所表示的主要化学成份相同的一组是( )
| A. | 大理石和石灰石 | B. | 生石灰和石灰石 | C. | 纯碱和烧碱 | D. | 冰和干冰 |
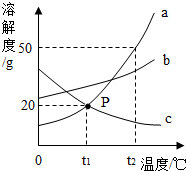 请根据图中a、b、c三种物质的溶解度曲线,回答下列问题:
请根据图中a、b、c三种物质的溶解度曲线,回答下列问题: