题目内容
5.下列实验操作正确的是( )| A. | 手持试管给试管里的物质加热 | |
| B. | 把鼻孔凑到容器口去闻气体的气味 | |
| C. | 给试管里的液体加热,液体体积一般不超过试管容积的$\frac{1}{3}$ | |
| D. | 用药匙取出块状固体 |
分析 A、手持试管给试管里的物质加热,会烫伤手;
B、根据实验室中“三不”原则分析;
C、根据加热试管内液体的注意事项分析;
D、取用块状固体药品用镊子.
解答 解:A、从实验的安全性考虑,手持试管给试管里的物质加热,会烫伤手,故A错误;
B、有些药品具有刺激性气味,有毒,所以不可把鼻孔凑到集气瓶口去闻气体的气味,故B错误;
C、给试管里的液体加热,液体体积一般不超越试管容积的$\frac{1}{3}$,故C正确;
D、取用块状固体药品要用镊子,故D错误.
故选C
点评 实验中一定要注意安全,实验基本规则中不允许的一定不要做,否则会造成不必要的伤害.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
15.有机酸是指一些具有酸性的有机化合物.下表是一些常见的有机酸:
则:
(1)X的化学式是C4H8O2;
(2)乙酸中,氧元素的质量分数最大.
| 甲酸 | 乙酸 | 丙酸 | 丁酸 | 戊酸 |
| CH2O2 | C2H4O2 | C3H6O2 | X | C5H10O2 |
(1)X的化学式是C4H8O2;
(2)乙酸中,氧元素的质量分数最大.
16.某化学兴趣小组探究稀盐酸与以下三种物质是否发生化学反应:
(1)甲、乙、丙三位同学设计了以下三个实验,请你填写相关内容:
(2)写出实验2的化学方程式:HCl+AgNO3 =HNO3 +AgCl↓
(3)在实验3中,因为没有明显实验现象,故无法判断该反应能否进行,为了证明该反应能否发生,甲、乙、丙三位同学又设计了如下实验方案,并继续进行实验.
【查阅资料】酸与碱发生中和反应会放出热量.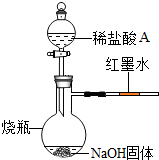
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸并不断震荡,同时测定溶液的pH,若测得溶液的pHb(填序号),则证明NaOH溶液与稀盐酸发生了化学反应.
a、逐渐增大并≥7 b、逐渐减小并≤7 c、始终不变并等于7
方案二:向NaOH溶液中滴加酚酞试液,溶液显红色,再滴加稀盐酸,若红色褪去,则证明NaOH溶液与稀盐酸发生了化学反应.
方案三:丙同学借助酸碱中和反应会放出热量,设计了如图所示的实验证明盐酸与氢氧化钠发生了反应,他观察到红墨水向右边(填“左”或“右”)移动.
【评价反思】有的同学提出,方案三的现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是:
①氢氧化钠固体溶于水会放出热量
②到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断
【拓展延伸】有位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,一会儿后红色消失了.①甲同学认为可能是酚酞溶液变质的缘故.你认为他的猜想是否合理?不合理(填“合理”或“不合理”)②乙同学认为可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故.丙同学认为乙同学的猜想不正确,他的理由是碳酸钠呈碱性.
| K2CO3溶液 | AgNO3溶液 | NaOH溶液 |
| 实验操作 | 实验现象 | 实验结论 | |
| 实验1 | 在K2CO3溶液中加入稀盐酸 | 有气泡产生 | 稀盐酸与K2CO3溶液 发生了化学反应 |
| 实验2 | 在AgNO3溶液加入稀盐酸 | 生成白色沉淀 | 稀盐酸与在AgNO3溶液发生了化学反应 |
| 实验3 | 在NaOH溶液加入稀盐酸 | 没有现象 | 无法判断该反应能否进行 |
(3)在实验3中,因为没有明显实验现象,故无法判断该反应能否进行,为了证明该反应能否发生,甲、乙、丙三位同学又设计了如下实验方案,并继续进行实验.
【查阅资料】酸与碱发生中和反应会放出热量.

【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸并不断震荡,同时测定溶液的pH,若测得溶液的pHb(填序号),则证明NaOH溶液与稀盐酸发生了化学反应.
a、逐渐增大并≥7 b、逐渐减小并≤7 c、始终不变并等于7
方案二:向NaOH溶液中滴加酚酞试液,溶液显红色,再滴加稀盐酸,若红色褪去,则证明NaOH溶液与稀盐酸发生了化学反应.
方案三:丙同学借助酸碱中和反应会放出热量,设计了如图所示的实验证明盐酸与氢氧化钠发生了反应,他观察到红墨水向右边(填“左”或“右”)移动.
【评价反思】有的同学提出,方案三的现象不足以证明NaOH与稀盐酸发生了化学反应,他的理由是:
①氢氧化钠固体溶于水会放出热量
②到底热量是氢氧化钠与盐酸反应放出的,还是氢氧化钠固体溶于水放出的,无法判断
【拓展延伸】有位同学向自己配制的氢氧化钠溶液中滴加酚酞试液时,溶液变红色,一会儿后红色消失了.①甲同学认为可能是酚酞溶液变质的缘故.你认为他的猜想是否合理?不合理(填“合理”或“不合理”)②乙同学认为可能是氢氧化钠溶液与空气中的二氧化碳反应的缘故.丙同学认为乙同学的猜想不正确,他的理由是碳酸钠呈碱性.
20.有关酒精灯的使用,下列说法不正确的是( )
| A. | 点燃酒精灯时不能用另一只酒精灯 | B. | 应用酒精灯的外焰给试管加热 | ||
| C. | 酒精灯的酒精量应超过容积的$\frac{2}{3}$ | D. | 熄灭酒精灯时用灯帽盖灭 |
15.某学习小组取氯酸钾与二氧化锰的混合物共3.3g,加热该混合物tmin后,冷却,称量剩余固体的质量,重复以上操作,依次称得4次加热后剩余固体的质量,记录数据如下:
请仔细分析实验数据,回答下列问题:
(1)表中a值为2.34,完全反应后产生氧气的质量为0.96g.
(2)该混合物中氯酸钾的质量是多少?
| 反应时间 | t | 2t | 3t | 4t | 5t |
| 剩余固体质量/g | 2.48 | 2.41 | 2.34 | a | 2.34 |
(1)表中a值为2.34,完全反应后产生氧气的质量为0.96g.
(2)该混合物中氯酸钾的质量是多少?
 近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题.
近日,网络上出现了“不锈钢水壶中的锰会让人智力低下”等传言.对此国家食品安全专家钟凯作了解答.“不锈钢材质中的锰含量与迁移量没有任何必然联系,合金状态下,金属的惰性会增强.”钟凯指出,食品接触材料的重金属迁移量是用强酸、强碱、有机溶剂等,在较高温度下长时间浸泡模拟出来的,如果这种状态下迁移量都没问题,日常使用根本不是问题. 去年12月28日,淮安有轨电车正式运营(如图所示),立即成为一道亮丽的风景线,请结合所学知识,回答以下问题:
去年12月28日,淮安有轨电车正式运营(如图所示),立即成为一道亮丽的风景线,请结合所学知识,回答以下问题: