题目内容
把铁片放硫酸铜溶液中,过一段时间后取出,在铁片上覆盖12﹒8克铜,求消耗铁片和硫酸铜各多少克?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:铁与硫酸铜反应生成铜和硫酸亚铁,利用反应的化学方程式,根据生成的铜的质量可以求得参加反应的铁和硫酸铜的质量.
解答:解:设消耗的铁片的质量为x,反应的硫酸铜质量是y
Fe+CuSO4═FeSO4+Cu
56 160 64
x y 12.8g
=
=
解得:x=11.2g y=32g
答:耗铁片为11.2g,硫酸铜的质量是32g.
Fe+CuSO4═FeSO4+Cu
56 160 64
x y 12.8g
| 56 |
| x |
| 160 |
| y |
| 64 |
| 12.8g |
解得:x=11.2g y=32g
答:耗铁片为11.2g,硫酸铜的质量是32g.
点评:本题考查根据方程式进行的计算,难度不大,属于基础性化学方程式计算的基础考查题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
实验室制备、收集氧气必须用到且齐全的一组仪器是( )
| A、试管、集气瓶、水槽 |
| B、试管、铁架台、单孔塞(带导管)、集气瓶、玻璃片 |
| C、试管、酒精灯、集气瓶 |
| D、试管、单孔塞(带导管)、酒精灯、集气瓶、玻璃片 |
下列实验操作中不正确的是( )
A、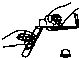 |
B、 |
C、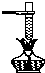 |
D、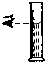 |
下列变化属于化学变化的是( )
| A、分离液态空气制氧气 |
| B、石墨制成金刚石 |
| C、活性炭使二氧化氮褪色 |
| D、石墨导电 |
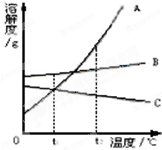 如图A、B、C为三种物质的溶解度曲线,据图回答:
如图A、B、C为三种物质的溶解度曲线,据图回答: