题目内容
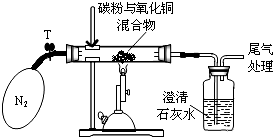 某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.
某学习小组对炭粉与氧化铜高温反应产物中气体的成分进行研究.【猜想】
①气体产物全部是CO2②气体产物全部是CO ③气体产物是
若猜想①成立,则碳和氧化铜高温反应的化学方程式为:
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量炭粉充分反应.通过参加反应的碳元素与氧元素的质量比.(提示:二氧化碳与一氧化碳中碳元素与氧元素的质量比分别为3:8和3:4)
【查阅资料】氮气不与碳、氧化铜产生反应,可用来隔绝氧气.
【实验】
| 操作步骤及实验现象 | 简答 |
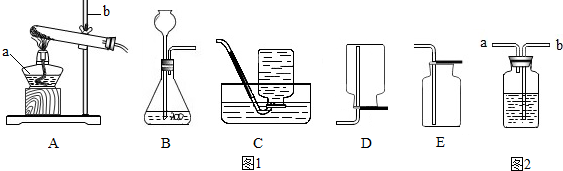
| ①称取8g氧化铜与2g炭粉均匀混合,放入重48.4g的玻璃管中,按上图装置连接 | / |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是 |
| ③夹紧T处弹簧夹,加热一段时间后,澄清石灰水变浑浊 | 澄清石灰水变浑浊的化学方程式为: |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为56.0g | / |
依据题目所给数据和质量守恒定律可得:反应生成的气体质量为
【结论】根据数据处理结果,得出猜想
考点:实验探究物质的组成成分以及含量,碳的化学性质,质量守恒定律及其应用,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:【猜想】根据质量守恒定律反应前后元素的种类不变可以猜想反应后得产物;
【实验】根据碳能与氧气反应分析通入氮气的目的,根据二氧化碳与氢氧化钙的反应写出反应的化学方程式
【数据处理】根据质量守恒定律反应前后元素的质量不变结合相关数据可以判断生成的组成.
【实验】根据碳能与氧气反应分析通入氮气的目的,根据二氧化碳与氢氧化钙的反应写出反应的化学方程式
【数据处理】根据质量守恒定律反应前后元素的质量不变结合相关数据可以判断生成的组成.
解答:解:【猜想】由质量守恒定律反应前后元素的种类不变,再一种情况是CO2和CO的混合物;若猜想①成立,则碳和氧化铜高温反应生成了铜和二氧化碳,反应的化学方程式为:C+2CuO
2Cu+CO2↑;
【实验】由于碳能与空气重工的氧气反应生成了二氧化碳.所以,先通入氮气能排出玻璃管内的空气,防止对实验造成干扰,目的是:排除玻璃管内空气对实验的干扰;
二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式是::CO2+Ca(OH)2=CaCO3↓+H2O
【数据处理】由于碳与氧化铜反应生成了铜和二氧化碳气体,根据质量守恒定律可得反应生成的气体质量为:48.4g+2g+8g-56.0g=2.4g.由题意可知,气体中的氧元素为1.6g,则气体中碳元素的质量为:2.4g-1.6g=0.8g.由于一氧化碳中碳元素和氧元素的质量比为:12:16.二氧化碳中碳元素和氧元素的质量比为:12:32.都不是0.8g:1.6g=1:2.所以气体是一氧化碳和二氧化碳的混合物.
【结论】由上述计算分析可知,猜想②成立.
故答为:CO和CO2;C+2CuO
2Cu+CO2↑;将玻璃管内的空气排尽;2.4;0.8;③.
| ||
【实验】由于碳能与空气重工的氧气反应生成了二氧化碳.所以,先通入氮气能排出玻璃管内的空气,防止对实验造成干扰,目的是:排除玻璃管内空气对实验的干扰;
二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,反应的化学方程式是::CO2+Ca(OH)2=CaCO3↓+H2O
【数据处理】由于碳与氧化铜反应生成了铜和二氧化碳气体,根据质量守恒定律可得反应生成的气体质量为:48.4g+2g+8g-56.0g=2.4g.由题意可知,气体中的氧元素为1.6g,则气体中碳元素的质量为:2.4g-1.6g=0.8g.由于一氧化碳中碳元素和氧元素的质量比为:12:16.二氧化碳中碳元素和氧元素的质量比为:12:32.都不是0.8g:1.6g=1:2.所以气体是一氧化碳和二氧化碳的混合物.
【结论】由上述计算分析可知,猜想②成立.
故答为:CO和CO2;C+2CuO
| ||
点评:本题主要考查了化学方程式的书写及其质量守恒定律的应用等方面的内容.完成此题可以依据物质的性质及题干提供的数据进行.

练习册系列答案
相关题目
正确量取12mL液体,应选用的一组仪器是( )
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
①15mL量筒 ②10mL量筒 ③20mL量筒 ④胶头滴管.
| A、③④ | B、①④ | C、②④ | D、①②④ |
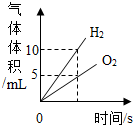
下列图象不能正确反映对应变化关系的是( )
 A A |  B | 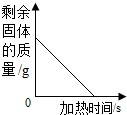 C |  D |
| A、电解水一段时间 |
| B、加热一定量高锰酸钾固体 |
| C、加热氯酸钾制氧气 |
| D、实验室利用双氧水制取氧气 |
根据下面四种粒子的结构示意图判断以下说法正确的是( )
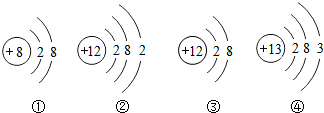

| A、①图是一种稀有气体元素的原子结构示意图 |
| B、②图所示的粒子是一种离子 |
| C、②③两图所示的粒子化学性质相似 |
| D、③④两图表示的是两种不同元素的粒子 |
下列混合气体点燃可能会发生爆炸的是( )
| A、CO和N2 |
| B、CO2和O2 |
| C、CO和O2 |
| D、H2和CO |
 化肥施用不当是引起水源污染的原因之一,我们必须学会科学施肥的方法.某生产碳酸氢铵(NH4HCO3) 化肥的企业,作了一个如图所示的大型户外广告.
化肥施用不当是引起水源污染的原因之一,我们必须学会科学施肥的方法.某生产碳酸氢铵(NH4HCO3) 化肥的企业,作了一个如图所示的大型户外广告.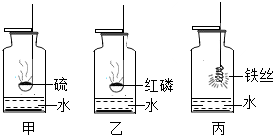 氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应.如图所示是硫粉、红磷、光亮的细铁丝在氧气中燃烧的实验装置:
氧气是一种化学性质比较活泼的气体,它可以和许多物质发生化学反应.如图所示是硫粉、红磷、光亮的细铁丝在氧气中燃烧的实验装置: