题目内容
15.若将含铁56%的铁钉10克与足量的硫酸铜溶液充分反应,则能生成多少克铜?分析 铁与硫酸铜溶液反应生成硫酸亚铁和铜,由参加反应的铁钉的质量、铁的质量分数,由反应的化学方程式列式计算出生成铜的质量.
解答 解:设生成铜的质量为x
Fe+CuSO4═FeSO4+Cu
56 64
10g×56% x
$\frac{56}{64}=\frac{10g×56%}{x}$ x=6.4g
答:生成6.4g铜.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,解题时要注意解题的规范性.

练习册系列答案
相关题目
5.下列变化都属于化学变化的是( )
| A. | 铁水铸成锅 | B. | 防毒面具中填充活性炭吸附毒气 | ||
| C. | 动植物的呼吸作用 | D. | 石油的分馏 |
6.全国各地多处出现雾霾天气,给人们生活带来了不少的影响,市政府采取措施,强制各用煤单位使用低硫优质煤,主要是为了防止下列哪种气体对空气的污染?( )
| A. | 二氧化碳 | B. | 一氧化碳 | C. | 二氧化硫 | D. | 二氧化氮 |
10.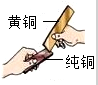 取黄铜片和铜片,观察光泽和颇色,按如图所示互相刻画.看哪种物质的硬度大
取黄铜片和铜片,观察光泽和颇色,按如图所示互相刻画.看哪种物质的硬度大
 取黄铜片和铜片,观察光泽和颇色,按如图所示互相刻画.看哪种物质的硬度大
取黄铜片和铜片,观察光泽和颇色,按如图所示互相刻画.看哪种物质的硬度大| 性质比较 | 物质 | |
| 黄铜 | 铜 | |
| 光泽和颜色 | 黄色 | 红色 |
| 硬度 | ||
| 结论 | ||
7.下列对物质颜色的描述不正确的是( )
| A. | 三氧化二铝是白色的 | B. | 氯化铁溶液是黄色的 | ||
| C. | 硫酸亚铁溶液是无色的 | D. | 硫酸铜溶液是蓝色的 |
15.2015年屠呦呦荣获诺贝尔化学奖,她于2011年发现青蒿素(青蒿素的化学式C15H22O5),这是一种用于治疗疟疾的药物,下列说法正确的是( )
| A. | 青蒿素中含有42个原子 | |
| B. | 青蒿素中C、H、O三种元素质量比15:22:5 | |
| C. | 青蒿素中碳元素的质量分数为63.8% | |
| D. | 青蒿素分子由C、H、O三种元素构成 |
 如图为电解水的装置,请根据实验的有关现象回答:
如图为电解水的装置,请根据实验的有关现象回答: