题目内容
13.莱芜素有“绿色钢城”之美誉,作为全国“钢铁十强企业”的莱钢集团为上海世博会各展馆的建设提供了数万吨钢铁材料.(1)莱钢炼铁厂常以焦炭、赤铁矿(主要成分是氧化铁)、空气等为主要原料炼铁,反应过程如图所示.其中焦炭的作用是燃烧放出热量,提供能量;与二氧化碳反应生成一氧化碳,提供还原剂;写出下列CO→Fe的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.

(2)电化学腐蚀是金属腐蚀的主要原因.当两种活泼性不同的金属在潮湿的环境中接触时,因形成原电池,活泼性强的金属首先被腐蚀.利用这一原理,为了保护轮船的钢质外壳,通常在行驶的轮船外壳上连接锌板(填“铜板”、“锌板”).
(3)钢铁防腐十分重要!请写出一种防止钢铁生锈的方法刷漆、涂油等.
分析 (1)从过程进行分析可以看出焦炭对过程提供了能量并为生成还原剂提供了原材料.
(2)根据题意在形成原电池时活泼性强的金属首先被腐蚀分析判断.
(3)根据防止铁生锈的措施分析回答;
解答 解:(1)焦炭在第一个环节中燃烧放出大量的热,提供了能量,第二环节则与二氧化碳反应生成了还原剂一氧化碳.炼铁发生的反应是:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(2)有题意可知,在形成原电池时活泼性强的金属首先被腐蚀,锌的活动性比铁强,而铜的活动性比铁要弱,为保护钢制外壳,一般应选择锌板.
(3)铁生锈的条件是铁与氧气和水接触,钢铁防腐十分重要!防止钢铁生锈的方法有刷漆、涂油等.
故答为:(1)燃烧放出热量,提供能量;与二氧化碳反应生成一氧化碳,提供还原剂,Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(2)锌板;(3)刷漆、涂油等.
点评 此题是一道关于铁的冶炼、防止腐蚀考查题,解题时主要依据题目提供的信息进行分析,属基础性知识考查题.

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
1.钛(Ti)是一种重要的航天金属材料.某学习小组对三种金属Ti、Al、Cu的金属活动性顺序进行探究.过程如下:
【提出假设】a.Ti金属活动性比Al强. b.Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,用砂布将表面擦光亮后分别投入等体积等质量分数的足量的稀盐酸中反应,观察现象.
【实验现象】
【实验结论】
(1)原假设中a不正确(填“a”、“b”或“ab”).
(2)三种金属的金属活动性由强至弱的顺序为Al>Ti>Cu.
【结论应用】不能 (填“能”或“不能”)用铝制容器来盛装波尔多液(含硫酸铜),理由是铝制容器能与硫酸铜溶液反应并置换出铜..
【提出假设】a.Ti金属活动性比Al强. b.Al金属活动性比Cu强.
【查阅资料】钛能与盐酸反应.
【实验设计】同温下,取大小相同的这三种金属薄片,用砂布将表面擦光亮后分别投入等体积等质量分数的足量的稀盐酸中反应,观察现象.
【实验现象】
| 金属 | Ti | Al | Cu |
| 与盐酸反应现象 | 反应缓慢 | 反应剧烈 | 无明显现象 |
(1)原假设中a不正确(填“a”、“b”或“ab”).
(2)三种金属的金属活动性由强至弱的顺序为Al>Ti>Cu.
【结论应用】不能 (填“能”或“不能”)用铝制容器来盛装波尔多液(含硫酸铜),理由是铝制容器能与硫酸铜溶液反应并置换出铜..
3.如图,这四位同学描述的可能是下面的同一个化学符号( )

| A. | H2O | B. | O3 | C. | NO2- | D. | HClO |
1.已知氮的某氧化物中,氮元素和氧元素的质量比是7:16,则该氮的氧化物的化学式可能是( )
| A. | NO | B. | N2O | C. | NO2 | D. | N2O3 |
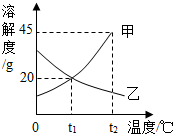 如图是甲、乙两物质的溶解度曲线图.t1℃时,12克甲物质放入50克水中形成的溶液质量是60克.甲乙两杯饱和溶液温度升高时能析出晶体的是乙物质(不考虑蒸发).
如图是甲、乙两物质的溶解度曲线图.t1℃时,12克甲物质放入50克水中形成的溶液质量是60克.甲乙两杯饱和溶液温度升高时能析出晶体的是乙物质(不考虑蒸发).