题目内容
6.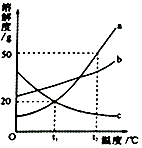 如图是a、b、c三种固体物质的溶解度曲线
如图是a、b、c三种固体物质的溶解度曲线(1)0℃时,a、b、c三种物质中,溶解度最小的是a.
(2)现a物质中含有少量b物质,可用降温(填“蒸发”或“降温”)结晶提纯得到a物质.
(3)将t1℃时三种物质的饱和溶液升温至t2℃时,所得溶液的溶质质量分数的由大到小关系是b>a>c(用“>”连接)
(4)t2℃时,将30ga物质放入50g水中,充分搅拌,所得溶液的溶质质量分数为33.3%.(保留一位小数).
分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
一种物质的溶解度受温度变化影响较大,一种物质的溶解度受温度变化影响较小,可以用降温结晶的方法分离;
溶液中溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%;
饱和溶液溶质质量分数=$\frac{溶解度}{100g+溶解度}$×100%.
解答 解:(1)0℃时,a、b、c三种物质中,溶解度最小的是a.
故填:a.
(2)由溶解度曲线可知,a的溶解度受温度变化影响较大,b的溶解度受温度变化影响较小,现a物质中含有少量b物质,可用降温结晶提纯得到a物质.
故填:降温.
(3)t1℃时,b的溶解度大于a的溶解度,a的溶解度等于c的溶解度,将t1℃时三种物质的饱和溶液升温至t2℃时,a和b白醋不饱和溶液,溶质质量分数都不变,c的溶解度减小,溶质质量分数减小,所得溶液的溶质质量分数的由大到小关系是b>a>c.
故填:b>a>c.
(4)t2℃时,a的溶解度是50g,将30ga物质放入50g水中,充分搅拌后只能够溶解25g,所得溶液的溶质质量分数为:$\frac{25g}{25g+50g}$×100%=33.3%.
故填:a;降温;b>a>c;33.3%.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.

练习册系列答案
 名师点拨卷系列答案
名师点拨卷系列答案 英才计划期末调研系列答案
英才计划期末调研系列答案
相关题目
4.金属在生产生活中用途广泛,下列有关金属的说法正确的是( )
| A. | 常温下所有金属都是固体 | |
| B. | 纯金属和其合金性能相差不大 | |
| C. | 在车船表面喷漆主要是为了防止金属锈蚀 | |
| D. | 废旧金属的回收利用没有实际价值 |
14.如表是KCl和KNO3在不同温度下的溶解度.下列说法不正确的是( )
| /℃ | 20 | 30 | 40 | 50 | |
| 溶解度/g | KCl | 34.0 | 37.0 | 40.0 | 42.6 |
| KNO | 31.6 | 45.8 | 6.9 | 85.5 | |
| A. | 20℃时,KCl的溶解度大于KNO3的溶解度 | |
| B. | 两种物质溶解度相等的温度在20~30℃之间 | |
| C. | 40℃时,5gKCl中加10g水可得33.3%溶液KNO3 | |
| D. | 50℃时,10g KNO3中加20g水,充分溶解后再降温到30℃,有KNO3固体析出 |
1.下列依据实验目的所设计的实验操作中,不合理的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去氢氧化钠溶液中少量氢氧化钙溶液 | 加入过量碳酸钠溶液,过滤 |
| B | 除去氯化钙溶液中少量稀盐酸 | 加入过量石灰石,过滤 |
| C | 鉴别羊毛和涤纶 | 灼烧并闻气味 |
| D | 鉴别真黄金和假黄金(铜锌合金) | 滴加稀盐酸 |
| A. | A | B. | B | C. | C | D. | D |
11.“一带一路”是跨越时空的宏伟构想,赋予古丝绸之路崭新的时代内涵.古丝绸之路将中国的发明和技术传送到外国.下列发明和技术不涉及化学变化的是( )
| A. | 烧制陶瓷 | B. | 火药爆炸 | C. | 蚕丝织布 | D. | 冶炼金属 |
15.下列实验方案,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 比较Fe、Cu和Ag的金属活动性 | 将Fe和Ag分别放入CuSO4溶液中 |
| B | 检验水垢中是否含有碳酸盐 | 取水垢加入稀盐酸,将气体通入澄清石灰水 |
| C | 鉴别石灰水和NaOH溶液 | 分别取少量溶液,滴加碳酸钠溶液 |
| D | 证明该气体为氢气 | 点燃,在火焰上罩一个干冷烧杯,内壁上出现无色液滴 |
| A. | A | B. | B | C. | C | D. | D |