题目内容
20. 某化学活动小组探究金属的反应规律.在室温条件下进行如图所示实验.
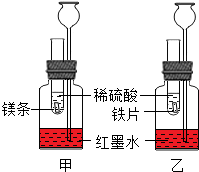
某化学活动小组探究金属的反应规律.在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小相同;同时加入等质量和等质量分数的稀硫酸,甲中反应的方程式为Mg+H2SO4=MgSO4+H2↑.
(1)若比较镁和铁的金属活动性,观察到的现象是镁和稀硫酸产生气泡的速率比铁和稀硫酸产生气泡的速率快;
(2)若比较相同时间内镁、铁与稀硫酸反应放出热量的多少,长颈漏斗中的现象是因为镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快.
(3)若实验所用的金属均过量,则甲装置中产生的H2的质量等于(填“大于”、“小于”或“等于”)乙装置中产生的H2质量.
分析 (1)金属越活泼,与稀盐酸或稀硫酸反应时速率越快,产生的气泡越多;
(2)考虑镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快;
(3)当金属过量时,与酸反应生成氢气的质量决定于酸的质量.
解答 解:试管内的镁条和铁片表面均被打磨洁净,且形状、大小相同;同时加入等质量和等质量分数的稀硫酸,甲中反应的方程式为:Mg+H2SO4=MgSO4+H2↑,
(1)因为镁比铁活泼,所以分别于等质量、等质量分数的稀硫酸反应时,镁和稀硫酸产生气泡的速率比铁和稀硫酸产生气泡的速率快.
(2)如图1所示实验的目的是:比较镁、铁分别与盐酸反应放热速度;因为镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快.
(3)若镁和铁均过量,则装置甲中产生的H2的质量等于装置乙中产生的H2质量.
故答案为:Mg+H2SO4=MgSO4+H2↑;
(1)镁和稀硫酸产生气泡的速率比铁和稀硫酸产生气泡的速率快.
(2)因为镁反应快放热多,因此甲中长颈漏斗里的液面上升得更快.
(3)等于.
点评 本题考查质量守恒定律的实验验验证和实验装置的选择,所以正确理解质量守恒定律和根据反应特点,即反应物和生成物中是否有气体或者烟雾,选择什么样的装置是解决本题的关键.

练习册系列答案
相关题目
10.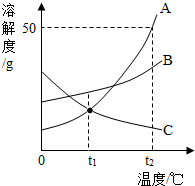 A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
 A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )
A、B、C三种物质的溶解度曲线如图所示.下列分析正确的是( )| A. | t2℃时,把30gA放入50g水中能得到A的饱和溶液,其中溶质和溶液的质量比为1:3 | |
| B. | 将t2℃时,A、B、C三种物质的饱和溶液降温至t1℃,所得溶液的溶质质量分数的大小关系是B>C=A | |
| C. | t1℃时,A、C两种物质的饱和溶液中溶质的质量相等 | |
| D. | 将C的饱和溶液变为不饱和溶液,可采用升温的方法 |
8.化学实验操作中常涉及“先后”问题,下列操作的先后顺序错误的是( )
| A. | 制取气体:先检验装置的气密性,后加入药品 | |
| B. | 点燃可燃性气体:先检验气体的纯度,后点燃 | |
| C. | CO还原氧化铁实验结束时:先停止通CO,后撤离酒精灯停止加热: | |
| D. | 除去N2中混有的CO和CO2:先通过灼热的氧化铜,再通过氢氧化钠溶液 |
5.两位同学围绕蜂窝煤燃烧进行了如下探究,其中依据质量守恒定律解释的是( )
| A. | 当煤燃烧正旺时将炉门关上,煤层上方发现蓝色火焰.解释:此时氧气不足而产生的一氧化碳在燃烧 | |
| B. | 煤燃烧完后煤灰的质量比煤的质量轻.解释:煤燃烧后产生二氧化碳等气体逸出 | |
| C. | 在煤炉上方放一壶水不能防止一氧化碳中毒.解释:一氧化碳难溶于水 | |
| D. | 将煤做成蜂窝状就更易燃烧.解释:蜂窝状的煤与空气接触面积增大 |
12.下列说法中,你认为正确的是( )
| A. | 如果两种粒子属于同一种元素,则它们原子核内的质子数一定相等 | |
| B. | 如果两种粒子属于同一种元素,则它们原子核内的中子数一定相等 | |
| C. | 如果两种粒子含有相同的质子数,则它们一定属于同一种元素 | |
| D. | 如果两种粒子含有相同的电子数,则它们一定属于同一种元素 |
10.下列实验方案能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 除去氧化钙中的碳酸钙 | 加入足量的水溶解,过滤 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 证明酸和碱恰好中和 | 向含有酚酞的氢氧化钠溶液中加入盐酸,溶液最终呈无色 |
| D | 测定久置于空气中的NaOH固体中碳酸钠的含量 | 取ag固体,加入足量稀盐酸,用排水法收集VmL气体 |
| A. | A | B. | B | C. | C | D. | D |
 金属是现代生活和工业生产中应用极为普遍的一类材料.
金属是现代生活和工业生产中应用极为普遍的一类材料.