题目内容
9.氮化镁是一种应用范围非常广泛的化合物,它可用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其它元素的氮化物,制备特殊的陶瓷材料等.氮化镁是浅黄色粉末,极易与水反应生成氢氧化镁沉淀和氨气;某兴趣小组用镁与氮气反应制备氮化镁(Mg3N2),取氮化镁样品16克按图1装置进行实验,测定氮化镁的纯度,发现B装置增重3.4克.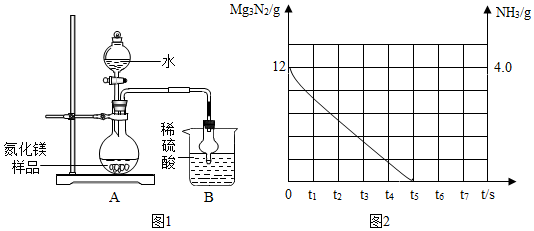
(1)求该样品中氮化镁的质量分数;
(2)导致该样品中氮化镁含量测定结果偏低的可能原因是氨气未能全部被吸收;
(3)经过精确测定,知道样品中氮化镁的质量分数为75%,请在图2画出生成的氨气质量的变化曲线.
分析 (1)稀硫酸能与氨气反应生成了硫酸铵,根据质量守恒定律B装置增重的质量就是生成的氨气的质量,由氨气的质量可求出氮化镁的质量,即可求出样品中氮化镁的质量分数;
(2)根据氨气未能全部被吸收分析回答;
(3)根据12g氮化镁与水反应生成氨气的质量画出氮化镁与生成氨气质量的变化曲线.
解答 解:(1)设样品中氮化镁的质量为x
Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
100 34
x 3.4g
$\frac{100}{34}=\frac{x}{3.4g}$ 解得:X=10g
样品中氮化镁的质量分数为:$\frac{10g}{16g}$×100%=62.5%
(2)导致该样品中氮化镁含量测定结果偏低的可能原因是氨气未能全部被吸收等;
(3)设12g氮化镁的完全分解生成的氨气的质量为y
Mg3N2+6H2O═3Mg(OH)2↓+2NH3↑
100 34
12g y
$\frac{100}{34}=\frac{12g}{y}$ 解得:y=4.08g,所以
所以生成的氨气质量的变化曲线为: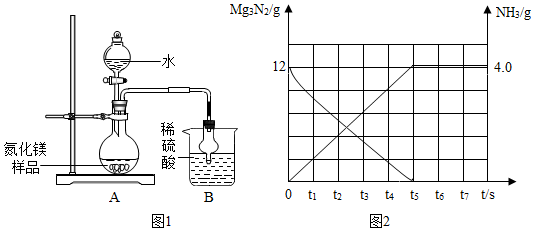
故答为:(1)该样品中氮化镁的质量分数是62.5%;(2)氨气未能全部被吸收;(3)见上图.
点评 本题属于根据化学方程式的计算,了解氨气能与稀硫酸反应生成了硫酸铵,正确判断出氨气的质量是解答本题的关键.

练习册系列答案
相关题目
20.下列有关空气的说法中,错误的是( )
| A. | 按质量计算,空气中含有氮气约 78%,氧气约 21% | |
| B. | 空气中各种成分的含量是相对稳定的 | |
| C. | 空气中的氧气可以供给呼吸、燃烧、炼钢、化工生产等 | |
| D. | PM2.5是造成空气污染的主要污染物之一 |
17.某氯化钾样品含有杂质氯化钙和氯化镁,设计提纯的流程图如下:

请认真分析流程中各步骤的信息作答:
(1)溶剂X是水(或H2O);Y溶液中溶质的化学式为:K2CO3.
(2)蒸发操作的目的是除去(填物质的化学式)H2O、HCl.
(3)写出加入过量KOH溶液反应的化学方程式:MgCl2+2KOH=Mg(OH)2↓+2KCl.
另有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种.为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示.表中“↓”表示有沉淀产生;“↑”表示有气体产生;“-”表示观察不到明显的现象变化.
回答下列问题:
(1)A中溶质的化学式是HCl,A与C反应的基本类型是复分解反应;
(2)A与B、B与C反应的化学方程式分别是2HCl+Na2CO3═2NaCl+CO2↑+H2O、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.

请认真分析流程中各步骤的信息作答:
(1)溶剂X是水(或H2O);Y溶液中溶质的化学式为:K2CO3.
(2)蒸发操作的目的是除去(填物质的化学式)H2O、HCl.
(3)写出加入过量KOH溶液反应的化学方程式:MgCl2+2KOH=Mg(OH)2↓+2KCl.
另有A、B、C三瓶失去标签的无色溶液,它们分别是盐酸、澄清石灰水和碳酸钠溶液中的一种.为了鉴别它们,各取少量溶液两两混合,实验结果如下表所示.表中“↓”表示有沉淀产生;“↑”表示有气体产生;“-”表示观察不到明显的现象变化.
| A | B | C | |
| A | ↑ | - | |
| B | ↑ | ↓ | |
| C | - | ↓ |
(1)A中溶质的化学式是HCl,A与C反应的基本类型是复分解反应;
(2)A与B、B与C反应的化学方程式分别是2HCl+Na2CO3═2NaCl+CO2↑+H2O、Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
4.下列是小强同学对有关知识的总结,其中完全正确的一组是( )
| A生活中的化学 | B物质的结构 |
| ①新装修屋内主要污染物--甲醛 ②形成酸雨的罪魁祸首--CO2 ③煤气中毒的原因--CO | ①氯化钠是由氯化钠分子构成的 ②金刚石是由金原子构成的 ③氮气是由氮分子构成的 |
| C化学中的守恒思想 | D物质的俗称 |
| ①加水稀释前后溶液的溶质质量不变 ②化学反应前后元素的种类和质量都不变 ③参与反应物质总质量等于生成物总质量 | ①Na2CO3:小苏打 ②C2H5OH:酒精 ③CaO:熟石灰 |
| A. | A | B. | B | C. | C | D. | D |
14.下列做法不能减轻雾霾程度的是( )
| A. | 植树造林 | B. | 洒水降尘 | C. | 燃放鞭炮 | D. | 共享单车出行 |
1.下列方法或试剂的使用能达到实验目的是( )
| A. | 干燥氧气-浓硫酸 | |
| B. | 区分黄金和黄铜-观察颜色 | |
| C. | 除去氧化钙中混有的氢氧化钙-水 | |
| D. | 验证质量守恒定律-铜与氯化镁溶液 |
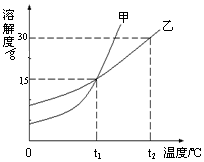 如图为甲、乙两物质的溶制度面线,回答下列问题.
如图为甲、乙两物质的溶制度面线,回答下列问题.