题目内容
14.下列实验操作错误的是( )| A. | 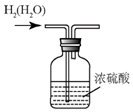 干燥氢气 干燥氢气 | B. | 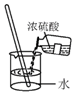 稀释浓硫酸 | C. | 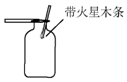 氧气的验满 氧气的验满 | D. | 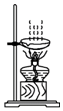 蒸发氯化钠溶液 |
分析 A.根据干燥气体的方法来分析;
B.根据稀释浓硫酸的方法来分析;
C.根据氧气的检验方法来分析;
D.根据蒸发结晶的注意事项来分析.
解答 解:A.用浓硫酸来干燥氢气时,气体从长管进入,通过浓硫酸后得以干燥,然后从短管排出,故A正确;
B.稀释浓硫酸时,要将浓硫酸沿着烧杯壁慢慢注入水中,并不断的用玻璃棒进行搅拌,故B正确;
C.氧气检验时,可将带火星的木条伸入集气瓶中,观察木条是否复燃即可,故C正确;
D.蒸发结晶时,要用酒精灯的外焰进行加热,且要用玻璃棒不断的进行搅拌,以防液体局部受热过高造成液滴飞溅,故D错误.
故选D.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 英才点津系列答案
英才点津系列答案 红果子三级测试卷系列答案
红果子三级测试卷系列答案
相关题目
5.科学的假设与猜想是科学探究的先导和价值所在.在下列假设(猜想)引导的探究肯定没有意义的是( )
| A. | 探究铁和硫酸铜溶液反应生成的气体可能是氢气 | |
| B. | 探究碳还原氧化铜的生成物可能有一氧化碳 | |
| C. | 探究铁锈的成分中可能含有氢氧化铁 | |
| D. | 探究滴加了酚酞的中和反应后的无色溶液中可能含有氢氧化钠 |
2.下列排顺不正确的是( )
| A. | 地壳中元素含量: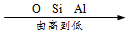 | B. | 物质的溶解性: | C. | 铁元素质量分数: | D. | 金属的活动性: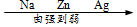 |
9.下列各组溶液,不用其他试剂就不能鉴别的是( )
| A. | MgSO4 BaCl2 Na2CO3 Na2SO4 | B. | Na2SO4 BaCl2 Na2CO3 HCl | ||
| C. | FeCl3 HCl NaOH KNO3 | D. | Ba(OH)2 Na2SO4 CuCl2 NaCl |
19.下列现象能用质量守恒定律解释的是( )
| A. | 蜡烛燃烧时慢慢变短 | |
| B. | 10 g食盐完全溶解于90 g水中,得到100 g食盐水 | |
| C. | 打开酒精的瓶盖一段时间,酒精质量变小 | |
| D. | 2体积的氢气加压后变成1体积 |
6.实验室制取二氧化碳,并证明生产的气体是二氧化碳,有下面几步:①向锥形瓶中装入碳酸钙;②检查装置气密性;③向长颈漏斗中注入酸液;④连接装置;⑤向试管中倒入澄清石灰水;⑥将产生的气体通入澄清石灰水.正确的顺序是( )
| A. | ⑤④③②①⑥ | B. | ②④⑤①③⑥ | C. | ④②①③⑤⑥ | D. | ④⑤②③①⑥ |
3.下列图示实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |
4. 小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是氢气.
(3)探究试管汇总剩余固体成分是什么?
【查阅资料】常见的铁的氧化物有FeO(黑色、没有磁性)、Fe2O3,Fe3O4
【初步验证】试管中固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4,猜想二:剩余固体是Fe与Fe3O4
【实验探究】
【实验结论】铁和水蒸气反应的化学方程式:3Fe+4H2O$\frac{\underline{\;高温\;}}{\;}$Fe3O4+4H2↑.
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.
 小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.
小杰同学在复习铁生锈条件时知道,常温下,没有氧气,铁与水几乎不反应,老师告诉同学们,高温下,铁与水蒸气能反应生产一种常见的铁的氧化物和一种气体,小杰很好奇,设计如图实验探究铁粉与水蒸气反应后的产物.(1)试管尾部放一团湿棉花的目的是提供水蒸气.
(2)探究生成的气体是什么?
用燃着的木条靠近肥皂泡,有爆鸣声,稍后有肥皂泡飘到空中,说明生成的气体是氢气.
(3)探究试管汇总剩余固体成分是什么?
【查阅资料】常见的铁的氧化物有FeO(黑色、没有磁性)、Fe2O3,Fe3O4
【初步验证】试管中固体为黑色,能全部被磁铁吸引.
【猜想与假设】猜想一:剩余固体是Fe3O4,猜想二:剩余固体是Fe与Fe3O4
【实验探究】
| 实验操作 | 实验现象结论 |
【反思与交流】该黑色固体不可能是Fe2O3,理由是Fe2O3是红棕色粉末.