题目内容
7.有一种无色无味液体A,在通电条件下分解产生两种气体B和C,已知铁丝可以在B中剧烈燃烧,火星四射,生成黑色固体物质D,C是自然界中最轻的气体,它在空气中燃烧生成A.(1)写出A、B、C、D四种物质的化学式:AH2O BO2 CH2 DFe3O4
(2)依次写出上文所涉及的化学反应方程式2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑,3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4,2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
分析 有一种无色无味液体A,在通电条件下分解产生两种气体B和C,结合水通电分解生成氢气和氧气,则A为水;BC为氢气、氧气中的一种;已知铁丝可以在B中剧烈燃烧,火星四射,生成黑色固体物质D,结合铁在氧气中燃烧,剧烈燃烧,火星四射,生成黑色固体物质四氧化三铁,则B为氧气,D为四氧化三铁;C是自然界中最轻的气体,C为氢气;据此进行分析解答.
解答 解:有一种无色无味液体A,在通电条件下分解产生两种气体B和C,结合水通电分解生成氢气和氧气,则A为水;BC为氢气、氧气中的一种;已知铁丝可以在B中剧烈燃烧,火星四射,生成黑色固体物质D,结合铁在氧气中燃烧,剧烈燃烧,火星四射,生成黑色固体物质四氧化三铁,则B为氧气,D为四氧化三铁;C是自然界中最轻的气体,C为氢气.
(1)A、B、C、D四种物质的化学式分别是H2O、O2、H2、.
(2)水通电分解生成氢气和氧气,反应的化学反应方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.
铁在氧气中燃烧生成黑色固体物质四氧化铁,反应的化学反应方程式为3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4.
氢气在空气中燃烧生成水,反应的化学反应方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
故答案为:(1)H2O;O2;H2;Fe3O4;(2)2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
点评 本题难度不大,解题时往往需要从题目中挖出一些明显或隐含的条件,抓住突破口(突破口往往是现象特征、反应特征等),获得结论,最后把结论代入原题中验证.

| A. | NaCl和AgNO3 | B. | H2SO4和Na2CO3 | C. | NaOH和HCl | D. | KNO3和Na2SO4 |
【提出问题】淡黄色固体物质的成分是什么?
【查阅资料】通过查阅资料,记录了下列几种物质的颜色:
小组成员一致认为产物中一定不含有氯化镁,理由是空气中无氯元素或空气中无氯气
【提出猜想】淡黄色的固体可能是Mg3N2.(填化学式)
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |

(2)C装置收集氮气的原因是除去装置B中的氧气
【实验结论】猜想是正确的.
【实验反思】本探究活动对物质燃烧新的认识是燃烧不一定都需要氧气 或 氮气也能支持燃烧.
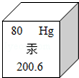 汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史很悠久,用途很广泛.在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )| A. | 汞属于非金属元素 | B. | 汞原子核外电子数是80 | ||
| C. | 汞原子核内中子数是200.6 | D. | 汞原子的相对原子质量是120.6 |
| A. | 柠檬酸属于氧化物 | B. | 柠檬酸含有6个碳元素 | ||
| C. | 柠檬酸中氧元素的质量分数最大 | D. | 柠檬酸中含有氧气 |

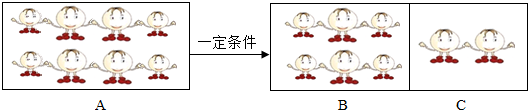
 ”表示氢原子,“
”表示氢原子,“ ”表示氧原子,若它们构成的分子在一定条件下发生如下图所示的变化.
”表示氧原子,若它们构成的分子在一定条件下发生如下图所示的变化.