题目内容
7.葡萄糖(C6H12O6)醋酸(CH3COOH)组成的混合物6g,在一定条件下完全燃烧,将生成的气体通过足量的澄清石灰水,生成沉淀的质量是( )| A. | 10g | B. | 6g | C. | 20g | D. | 无法计算 |
分析 根据葡萄糖(C6H12O6)醋酸(CH3COOH)分子中碳原子、氢原子和氧原子的个数比均为1:2:1,计算出6g混合物碳元素的质量,进而结合质量守恒定律,反应前后碳元素的质量不变,化合物的质量=该化合物中某元素的质量÷该元素的质量分数,进行分析解答.
解答 解:葡萄糖(C6H12O6)醋酸(CH3COOH)分子中碳原子、氢原子和氧原子的个数比均为1:2:1,则6g混合物碳元素的质量为6g×$\frac{12}{12+1×2+16}$×100%=2.4g.
由质量守恒定律,反应前后碳元素的质量不变,在一定条件下完全燃烧,将生成的气体通过足量的澄清石灰水,生成碳酸钙沉淀的质量是2.4g÷($\frac{12}{40+12+16×3}×$100%)=20g.
故选:C.
点评 本题难度不大,找出葡萄糖(C6H12O6)醋酸(CH3COOH)分子中碳原子、氢原子和氧原子的个数比均为1:2:1是正确解答本题的关键.

练习册系列答案
相关题目
12.下列说法正确的是( )
| A. | 空气中氧气的体积分数最大 | |
| B. | 用灯帽盖灭酒精灯是因为降低了可燃物温度 | |
| C. | 淡水资源丰富,所以淡水资源可以取之不尽,用之不竭 | |
| D. | 使用新型可降解塑料可减少“白色污染” |
9.我国探月工程已经发现月球中含有种类繁多的矿物,其中有的是在地球上未曾发现过的矿产.下列月球矿物中属于单质的是( )
| A. | 钛铁矿 | B. | 铁锡合金 | C. | 纯铁颗粒 | D. | 硫化银颗粒 |
2.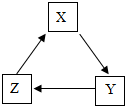 下列各组物质间通过一步反应就能实现如图转化的是( )
下列各组物质间通过一步反应就能实现如图转化的是( )
 下列各组物质间通过一步反应就能实现如图转化的是( )
下列各组物质间通过一步反应就能实现如图转化的是( ) | X | Y | Z | |
| A | Ca(OH)2 | CaCO3 | CaO |
| B | AgNO3 | Ba(NO3)2 | BaSO4 |
| C | Cu | CuO | CuCl2 |
| D | Fe2O3 | Fe | FeCl2 |
| A. | A | B. | B | C. | C | D. | D |
16.下列关于活中常用材料的认识正确的是( )
| A. | 涤纶、羊毛和棉花都是天然纤维 | |
| B. | 各种塑料在自然界中都不能降解 | |
| C. | 用铁桶盛放稀硫酸 | |
| D. | 不锈钢属于合金材料,具有较强的抗腐蚀性 |
17.下列物质的转化过程不符合A?B→C的是( )
| A. | CO?CO2→CaCO3 | B. | CO2?C6H12O6→H2O | C. | O2?H2O→H2 | D. | Cu?CuO→Cu(OH)2 |