题目内容
13. 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.
请分析回答下列问题:
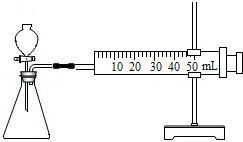
(1)连接仪器组装成如右图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?不漏气.
(2)根据下表中的现象填写结论.
| 金属 | 铁 | 铅 |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度较快 |
| 结论 | 铅比铁的金属活动性强 | |
(3)除了比较与酸反应产生气体速度的快慢,你还有其他化学方法可以比较金属活动性的强弱吗?请举出一种方法(写出原理即可)Pb+FeCl2=Fe+PbCl2.
分析 (1)根据检查装置气密性的原理分析;
(2)根据金属与酸反应的速度可以比较金属活动性强弱;
(3)根据金属是否能与盐溶液反应可以比较金属活动性强弱.
解答 解:(1)如果装置不漏气,针筒的活塞被拉出一段后,针筒内压强变小,在大气压的作用下,活塞一段时间后又回到原来的位置;
(2)由表中信息可知,铁与酸反应不如铅与酸反应快,故铅比铁的金属活动性强;铁与稀盐酸反应生成氯化亚铁和氢气;
(3)比较金属活动性强弱还可用金属是否能与盐溶液反应来比较,如铅与氯化亚铁溶液反应生成铁和氯化铅,说明铅的活动性比铁强.
答案:(1)不漏气;(2)铅比铁的金属活动性强; Fe+2HCl=FeCl2+H2↑;
(3)Pb+FeCl2=Fe+PbCl2.
点评 本题是一道综合知识题目,考查的角度较广,难度较大,要求学生具有分析和解决问题的能力.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案
相关题目
1.下列各组物质在给定条件下能大量共存的是( )
| A. | 在 pH=1 的溶液中:KCl、Na2SO4、HNO3 | |
| B. | 在 pH=2 的溶液中:NaCl、Na2CO3、Na2SO4; | |
| C. | 在 pH=13 的溶液中:FeCl3、Ba ( NO3 )2、CaCl2 | |
| D. | 在 pH=14 的溶液中:BaCl2、Na2CO3、NaOH |
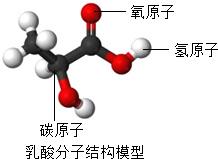 酸奶是以新鲜全脂牛奶为原料,经乳酸菌发酵制成的乳制品.酸奶中含有的乳酸对健康是有益的.乳酸分子(C3H6O3)的结构模型如图所示.请回答下列问题:
酸奶是以新鲜全脂牛奶为原料,经乳酸菌发酵制成的乳制品.酸奶中含有的乳酸对健康是有益的.乳酸分子(C3H6O3)的结构模型如图所示.请回答下列问题: