题目内容
向100g水中不断加入固体A或改变温度,得到相应的溶液①~⑤。下列说法正确的是( )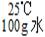
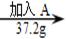 ①
① 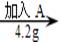 ②
② 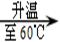 ③
③ 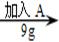 ④
④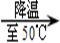 ⑤
⑤
资料:A的溶解度
| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| 溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |
C.②中A的质量分数最大 D.①③④⑤为不饱和溶液
B
解析试题分析:根据固体物质A的溶解度分析。
A、结合图表中数据可知,A的溶解度随温度的升高而增大,故25℃时A物质的溶解度应大于37.2g而小于41.4g,而溶液②是在25℃时,在100g水中加入了37.2g+4.2g=41.4g的A物质,故一定是饱和溶液;溶液④是60℃时,在100g水中加入了41.4g+9g=50.4g的A物质,而此温度下A的溶解度为55.2g,故溶液④为不饱和溶液;再降温到50℃时,溶解度恰好变为55.2g,故溶液⑤恰好为饱和溶液,错误;
B、由于溶液由60℃降温到50℃时,没有溶质析出(恰好饱和),故④⑤中的溶质质量都为50.4g,溶剂的质量都为100g,所以二者的质量分数相同,正确;
C、五种溶液中的溶剂的质量都是100g,①中的溶质为37.2g,②中的溶质大于37.2g,小于 41.4g,③中的溶质为41.4g,④中的溶质为50.4g,⑤中的溶质为50.4g,故②中A的质量分数不是最大的,错误;
D、25℃时A物质的溶解度要大于37.2g小于41.4g,而①中加入的溶质为37.2g,所以该温度下①溶液为不饱和溶液;60℃时A物质的溶解度为55.2g,而此时溶液中的溶质质量为41.4g,故为不饱和溶液,但结合上面的分析可知,溶液⑤恰好为饱和溶液,错误。故选B
考点:固体溶解度的影响因素,饱和溶液和不饱和溶液,溶质的质量分数、溶解性和溶解度的关系
点评:判断某温度下的溶液是否饱和,关键是看在该温度下该物质的溶解度是多少,而该温度下溶液中又到底溶解了多少的该溶质。

练习册系列答案
相关题目
 28、下列数据是硝酸钾固体在不同温度时的溶解度.
28、下列数据是硝酸钾固体在不同温度时的溶解度. 下列数据是固体A在不同温度时的溶解度.
下列数据是固体A在不同温度时的溶解度.