题目内容
14.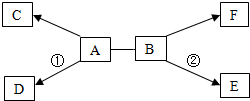 A-F是初中化学常见的六种物质,已知A广泛用于造纸、玻璃、洗涤剂生产等工业,C和F都是无色气体,且F是单质,反应①和②都有白色沉淀生成.它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示两种物质能相互反应;部分反应物、生成物及反应条件未标出).请回答下列问题:
A-F是初中化学常见的六种物质,已知A广泛用于造纸、玻璃、洗涤剂生产等工业,C和F都是无色气体,且F是单质,反应①和②都有白色沉淀生成.它们之间的关系如图所示(“→”表示物质间的转化关系,“-”表示两种物质能相互反应;部分反应物、生成物及反应条件未标出).请回答下列问题:(1)写出下列物质的化学式:ANa2CO3、FH2;
(2)若D是一种常见的碱,则反应①的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)若B是人体胃液中的主要成分,则反应②的化学方程式为HCl+AgNO3=AgCl↓+HNO3.
分析 根据A~F是初中化学常见的六种物质,根据“已知A广泛用于造纸、玻璃、洗涤剂生产等工业”,则推测A为碳酸钠,根据“C和F都是无色气体,且F是单质,反应①和②都有白色沉淀生成”,根据“若B是人体胃液中的主要成分”,则推测B为稀盐酸,结合图框,C和F都是无色气体,A会转化成C,所以C是二氧化碳,盐酸会生成无色气体F,则推测C和F分别为二氧化碳、氢气,则反应①为碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;反应②为稀盐酸与硝酸银溶液反应生成氯化银沉淀和硝酸,E可以是氯化银沉淀.推出的各种物质都满足题中的转化关系,推导合理.
解答 解:根据A~F是初中化学常见的六种物质,根据“已知A广泛用于造纸、玻璃、洗涤剂生产等工业”,则推测A为碳酸钠,根据“C和F都是无色气体,且F是单质,反应①和②都有白色沉淀生成”,根据“若B是人体胃液中的主要成分”,则推测B为稀盐酸,结合图框,C和F都是无色气体,A会转化成C,所以C是二氧化碳,盐酸会生成无色气体F,则推测C和F分别为二氧化碳、氢气,则反应①为碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠;反应②为稀盐酸与硝酸银溶液反应生成氯化银沉淀和硝酸,E可以是氯化银沉淀,推出的各种物质都满足题中的转化关系,推导合理;则:
(1)根据分析,A为碳酸钠,F为氢气,故A、F物质的化学式分别为:Na2CO3、H2;
(2)若D是一种常见的碱,则D为碳酸钙,则反应①为碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,其化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)若B是人体胃液中的主要成分,则B为稀盐酸,则反应②是盐酸和硝酸银反应生成氯化银沉淀和硝酸,化学方程式为:HCl+AgNO3=AgCl↓+HNO3;
故答案为:
(1)Na2CO3、H2;
(2)Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
(3)HCl+AgNO3=AgCl↓+HNO3.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

| A. | 尿素C0(NH2)2 | B. | 磷酸二氢钙Ca(H2PO4)2 | ||
| C. | 磷酸二氢铵NH4H2PO4 | D. | 氯化钾KCl |
| 清洁产品 | 除垢净 | 去污粉 | 管道通 |
| 主要成分 | 盐酸 | 碳酸钠 | 氢氧化钠、铝粉 |
(2)去污粉与除垢净不能混合使用,其原因是Na2CO3+2HCl═2NaCl+CO2↑+H2O(用化学方程式表示).
(3)管道通使用时不能接触皮肤,原因是NaOH具有强烈的腐蚀性.使用时利用Al与NaOH溶液反应放出大量的热,以加快NaOH与淤积物的作用,该反应的化学方程式为2Al+2NaOH+2H2O═2NaAlO2+3H2↑,其中铝元素的化合价变化为0~+3.
| 实验操作(可用文字叙述,也可用图示) | 实验现象 |