题目内容
在由C、FeO、Fe3O4组成的混合物中,已知该混合物中氧元素的质量分数为16%,则该混合物中碳元素的质量分数可能为( )
| A、28% | B、42% |
| C、35% | D、45% |
考点:元素的质量分数计算
专题:化学式的计算
分析:可用极端假设法,1、假设为FeO、C的混合物,2、假设为Fe3O4和C的混合物,令混合物的总质量为100g,根据铁的氧化物中铁元素与氧元素质量关系计算铁的氧化物含有氧元素的质量,进而计算碳的质量和碳的质量分数,实际碳的质量分数介于这两种情况之间.
解答:解:假设混合物共100g,
设混合物只有FeO和C,则含O氧元素质量16g,则与Fe结合的为56g,C的质量为100g-56g-16g=28g,故碳的质量分数为28%;
同理若为Fe3O4和C的混合物,则含O元素质量为16g,与O元素结合的Fe的质量16g×
=42g,应该含C的质量为100g-16g-42g=42g,碳酸钙的质量分数为42%,
所以C的质量分数介于28%~42%之间,
故选:C.
设混合物只有FeO和C,则含O氧元素质量16g,则与Fe结合的为56g,C的质量为100g-56g-16g=28g,故碳的质量分数为28%;
同理若为Fe3O4和C的混合物,则含O元素质量为16g,与O元素结合的Fe的质量16g×
| 56×3 |
| 16×4 |
所以C的质量分数介于28%~42%之间,
故选:C.
点评:本题考查混合物的有关计算,难度中等,注意利用极限法确定碳的质量分数范围.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
元素符号是为了书写和学术交流的方便,国际上统一采用的一种符号,下列元素符号书写正确的是( )
| A、AL | B、mG | C、cl | D、Cu |
下列溶液中通入(或加入)括号中的物质,能使溶液的pH明显增大的是( )
| A、饱和的石灰水(CO2) |
| B、稀硫酸(BaCl2) |
| C、氯化钙的饱和溶液(Na2CO3) |
| D、稀盐酸(NaOH) |
下列各组物质中,化学性质差别最大的一组是( )
| A、金刚石、石墨 |
| B、红磷、白磷 |
| C、氧气、臭氧 |
| D、一氧化碳、二氧化碳 |
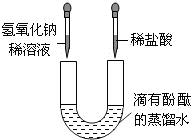 U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示).下列说法正确的是( )
U形管中是滴有酚酞试液的蒸馏水,向左、右两管中分别同时逐滴滴加一定量的氢氧化钠稀溶液和稀盐酸(如图所示).下列说法正确的是( )| A、开始时左边溶液呈蓝色,右边溶液呈红色 |
| B、开始时左边溶液呈无色,右边溶液呈红色 |
| C、刚好完全反应时U形管中溶液一定呈红色 |
| D、刚好完全反应时U形管中溶液一定呈无色 |
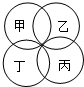 在以下的“四连环”图中,每环代表一种物质,相连环间所代表的物质在一定条件下可以发生反应,下表的选项中,符合这一要求的是( )
在以下的“四连环”图中,每环代表一种物质,相连环间所代表的物质在一定条件下可以发生反应,下表的选项中,符合这一要求的是( )
