题目内容
14.课外小组同学利用图A、图B所示装置验证碳酸钠的性质.(1)利用图A装置进行如下实验

步骤一:向三口瓶内的碳酸钠溶液中滴加酚酞,溶液显红色.
步骤二:将注射器1的针头向瓶内推进,使针头下端进入瓶内液面下,向外拉注射器,此时注射器1中反应的化学方程式为Na2CO3+Ca(OH)2=CaCO3↓+2NaOH,看到明显现象后,将针头向上拉至图示所示位置.
步骤三:验证碳酸钠是碳酸盐,应该进行的实验操作是将注射器2中稀硫酸推入瓶中,看到的实验现象是瓶中产生气泡,烧杯中澄清石灰水变浑浊.
(2)利用图B装置进行实验.将二氧化碳持续通入饱和碳酸钠溶液中,发生反应为:Na2CO3+CO2+H2O=2NaHCO3↓,产生浑浊的原因是除反应消耗水使溶剂量减少外,还有的其它原因是20℃时,碳酸氢钠的溶解度小于碳酸钠;生成碳酸氢钠的质量大于参加反应的碳酸钠的质量(请依据下表信息回答).
| 物质 | 20℃时溶解度/g | 相对分子质量 |
| Na2CO3 | 21.5 | 106 |
| NaHCO3 | 9.6 | 84 |
分析 (1)根据碳酸钠与氢氧化钙的反应原理来分析;根据碳酸根离子的检验方法来分析;
(2)根据化学方程式以及表格数据来分析.
解答 解:(1)步骤二:碳酸钠溶液与氢氧化钙溶液反应生成碳酸钙白色沉淀和氢氧化钠,观察到石灰水变浑浊;故填:Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
步骤三:碳酸钠能与酸反应生成二氧化碳气体,所以可将注射器2中的稀硫酸推入瓶内,若观察到瓶内产生气泡,且烧杯中的澄清的石灰水变浑浊,则证明碳酸钠是碳酸盐;故填:将注射器2中稀硫酸推入瓶中;瓶中产生气泡,烧杯中澄清石灰水变浑浊;
(2)由Na2CO3+CO2+H2O=2NaHCO3↓可知,产生浑浊的原因是除反应消耗水使溶剂量减少外,还有20℃时,碳酸氢钠的溶解度小于碳酸钠;生成碳酸氢钠的质量大于参加反应的碳酸钠的质量.故答案为:20℃时,碳酸氢钠的溶解度小于碳酸钠;生成碳酸氢钠的质量大于参加反应的碳酸钠的质量.
点评 本题考查了物质的检验,化学方程式的书写,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
4.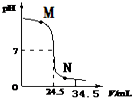 某同学做稀硫酸与氢氧化钠溶液反应实验,右图是烧杯中溶液的pH随所滴加的溶液
某同学做稀硫酸与氢氧化钠溶液反应实验,右图是烧杯中溶液的pH随所滴加的溶液
体积的变化而变化的关系图.根据图示,下列说法正确的是( )
 某同学做稀硫酸与氢氧化钠溶液反应实验,右图是烧杯中溶液的pH随所滴加的溶液
某同学做稀硫酸与氢氧化钠溶液反应实验,右图是烧杯中溶液的pH随所滴加的溶液体积的变化而变化的关系图.根据图示,下列说法正确的是( )
| A. | M点溶液中溶质为H2SO4和Na2SO4 | |
| B. | 若同时测量反应过程中温度,当滴加溶液的体积为34.5mL时,溶液温度最高 | |
| C. | 实验过程中,在溶液中滴入酚酞试液,溶液不变红色,说明反应恰好完成 | |
| D. | 取N点的溶液,滴入过量的硝酸钡溶液,有白色沉淀产生,过滤,滤液中的溶质有3种 |
5.下列实验操作不能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 除去CO2中少量的CO | 将混合气体通过灼热的氧化铜 |
| B | 鉴别Fe2O3和Fe3O4 | 观察颜色 |
| C | 除去NaHCO3中少量Na2CO3 | 将固体加热至质量不再减少 |
| D | 除去KCl中少量MnO2 | 将混合物先溶解再过滤,然后蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
2.下列过程中发生化学变化的是( )
| A. |  鲜花变色 | B. |  酒精挥发 | ||
| C. |  活性炭净水 | D. |  水果榨汁 |
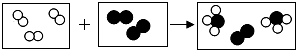 用“
用“ ”和“
”和“ ”代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生反应生成新物质X,微观过程如图所示.下列说法正确的是A
”代表两种不同单质A2和B2的分子,A2和B2在一定条件下发生反应生成新物质X,微观过程如图所示.下列说法正确的是A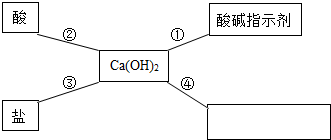 对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应.
对知识的归纳和总结是学好科学的重要方法.在学习了碱的性质后,小红同学总结了氢氧化钙的四条化学性质(如图),即氢氧化钙与图中四类物质能够发生化学反应. 是某些非金属氧化物.
是某些非金属氧化物.