题目内容
19.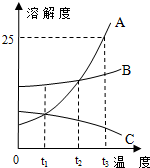 A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:(1)t3℃时将20g A物质放入50g水中,充分搅拌,所得溶液中溶质与溶剂质量比是1:4;
(2)若B中混有少量的A,最好采用蒸发结晶(或蒸发溶剂)的方法提纯B;
(3)t3℃时,将等质量的A、B、C三种物质加水溶解配制成饱和溶液,所得溶液质量由大到小的顺序是C>B>A.
分析 (1)根据物质的溶解度曲线,分析确定:t3℃时,A的溶解度溶解度解答;
(2)根据A的溶解度随温度变化而变化的情况进而确定结晶析出的方法解答;
(3)据该温度下三种物质的溶解度大小分析解答.
解答 解:
(1)t3℃时,A的溶解度溶解度为25g,100g水中溶解25g,将20g A物质放入50g水中,只能溶解12.5gA,所得溶液中溶质与溶剂的质量比是12.5g:50g=1:4;
(2)从题目提供的信息可得:A物质的溶解度受温度影响很大,提纯A最好用降温结晶,B的溶解度受温度影响较小,得到B的晶体,最好采用蒸发结晶;
(3)t3℃时,A、B、C三种物质的溶解度由大到小的顺序是A、B、C,所以将等质量的A、B、C三种物质加水溶解配制成饱和溶液所需水的质量A<B<C,所得溶液质量的大小关系为C>B>A.
故答案是:
(1)1:4;
(2)蒸发结晶(或蒸发溶剂);
(3)=
(4)C>B>A.
点评 本题难度不大,主要考查了固体溶解度曲线所表示的意义,通过本题可以加强学生对固体溶解度的理解,培养学生应用知识解决问题的能力.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
7.除去下列物质中的杂质(括号内为杂质),所选用试剂及操作方法均正确的是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | NaCl(Na2CO3) | CaCl2溶液 | 加适量CaCl2溶液,过滤、将滤液蒸发结晶 |
| B | Na2SO4(NaOH) | 稀盐酸 | 加过量稀盐酸、蒸发结晶 |
| C | KCl(KClO3) | MnO2 | 加MnO2,加热后冷却 |
| D | Fe2(SO4)3溶液(CuSO4) | 过量铁粉 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
14.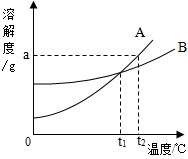 如图是A、B两种固体物质的溶解度曲线.下列说法中错误的是( )
如图是A、B两种固体物质的溶解度曲线.下列说法中错误的是( )
 如图是A、B两种固体物质的溶解度曲线.下列说法中错误的是( )
如图是A、B两种固体物质的溶解度曲线.下列说法中错误的是( )| A. | t2℃时,A的饱和溶液中溶质的质量分数为a÷100×100% | |
| B. | 将t2℃时B的饱和溶液降温到t1℃时,溶液变稀了 | |
| C. | A、B的溶解度都随温度升高而增大 | |
| D. | t1℃时A、B的溶解度相等 |
4.工业上利用乙炔(C2H2)产生的灰浆和残渣制备化工原料KClO3和超细CaCO3.
生产流程为:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{置露于空气}{→}$残渣.
资料:电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(1)残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:
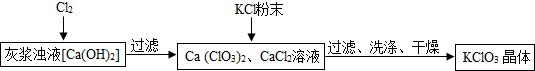
(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
上述流程中加入KCl粉末,KCl与Ca(ClO3)2(填化学式)发生了复分解反应,得到KClO3晶体.你认为能得到KClO3晶体的原因是相同温度下,氯酸钾的溶解度小.
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐):
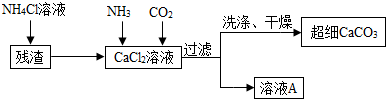
(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
生产流程为:电石(CaC2)$\stackrel{水}{→}$灰浆$\stackrel{置露于空气}{→}$残渣.
资料:电石与水的反应为:CaC2+2H2O=Ca(OH)2+C2H2↑.
(1)残渣中主要成分是Ca(OH)2和CaCO3.
Ⅰ.制备KClO3的流程如下:

(2)向灰浆浊液中通入Cl2,得到Ca(ClO3)2、CaCl2溶液.反应中Ca(ClO3)2与CaCl2的化学计量数分别为1和5.写出此反应的化学方程式6Ca(OH)2+6Cl2=Ca(ClO3)2+5CaCl2+6H2O.
(3)有关物质在常温下的溶解度如下:
| 物质 | Ca(ClO3)2 | CaClO3 | KClO3 | KCl |
| 溶解度/g | 209.0 | 74.5 | 7.3 | 34.2 |
(4)洗涤时,可选用下列BC洗涤剂(填字母编号).
A、KCl饱和溶液 B、冰水 C、饱和KClO3溶液
Ⅱ.制备超细CaCO3的流程如下(注:加入NH4Cl的目的是溶解残渣中的难溶盐):

(5)流程中溶液A可循环使用,其主要成分的化学式是NH4Cl.
11.如表所示实验操作中,不能达到实验目的是( )
| 实验目的 | 实验操作 | |
| A | 鉴别纯棉制品和羊毛面料 | 分别取样灼烧、闻气味 |
| B | 提纯含少量泥沙的粗盐 | 将粗盐加适量水溶解、过滤、蒸发结晶 |
| C | 除去氯化钙溶液中少量盐酸 | 加入过量的碳酸钙粉末、充分反应后过滤 |
| D | 分离硫酸钠和硫酸锌的混合溶液 | 加入过量氢氧化钠溶液,充分反应后过滤 |
| A. | A | B. | B | C. | C | D. | D |
8.下列矿石的主要成分表达错误的是( )
| A. | 黄铁矿(FeS2) | B. | 菱铁矿(FeCO3) | C. | 黄铜矿(CuFeS2) | D. | 磁铁矿(FeS) |
18.下列化学反应属于置换反应的是( )
| A. | Cu+2AgNO3═Cu(NO3)2+2Ag | B. | NaOH+HCl═NaCl+H2O | ||
| C. | Fe2O3+6HCl═2FeCl3+3H2O | D. | SO2+2NaOH═Na2SO3+H2O |