题目内容
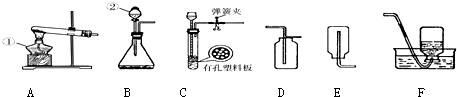
17.某学生在进行二氧化碳的制取和性质实验时,经过认真分析研究,对课本中的气体发生装置(图A)进行了改进(图B).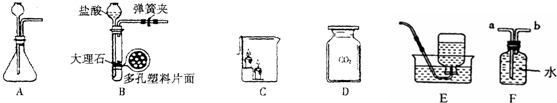
(1)如何检查A装置的气密性:在右导管口连一乳胶管,在乳胶管上夹弹簧夹,向长颈漏斗内加水,至形成液封,再加适量水,静置一段时间后,若长颈漏斗液面与试管内液面差保持不变,说明气密性良好.
(2)改进后装置的优点是随开随制,随关随停.
(3)写出B中发生反应的化学方程式CaCO3+2HCl=CaCl2+CO2↑+H2O.
(4)D中的CO2倒入C中做性质实验时,操作方法是(按教材回答)将二氧化碳沿烧杯壁慢慢倒入,观察到的现象是蜡烛由低到高依次熄灭.此实验说明二氧化碳具有不能燃烧也不支持燃烧且密度比空气大的性质.
(5)如何检验D中的气体是CO2CO2+Ca(OH)2=CaCO3↓+H2O(用化学方程式表示)
(6)用A装置制O2时,发生的化学方程式是2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(7)E装置适合收集气体的性质有难溶于水且不和水反应,如果某同学用F装置收集尾气一氧化碳,则收集时气体应从导管口的b 端(填“a”或“b”)通入.
(8)某同学利 用收集的二氧化碳气体,设计了如下一组实验.取四朵用石蕊试液染成的紫色的干燥纸花,分别按下图进行实验,向花分别喷洒稀盐酸或水.回答下列问题:
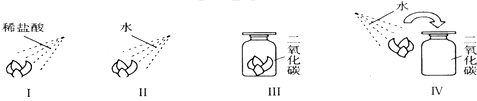
①观察到纸花的颜色变化是Ⅰ:纸花变红;Ⅱ:纸花不变色;Ⅲ:纸花不变色;Ⅳ:纸花变红;
②该同学进行的Ⅰ、Ⅱ两项实验,说明什么?使纸花变红是酸不是水.
③该同学进行四组对比实验的目的是什么?(用文字叙述)二氧化碳不能使石蕊变色,二氧化碳的水溶液能使石蕊变红.
④写出实验Ⅳ中发生反应的化学方程式:CO2+H2O═H2CO3.
分析 (1)根据装置气密性的检验方法来分析;
(2)对课本中的气体发生装置(图A)进行了改进(图B).添加了有孔塑料板,使得固体药品与液体药品可以分离;改变了装置A中药品一接触就直接反应的不足;
(3)碳酸钙和稀盐酸反应生成了氯化钙、水和二氧化碳,可以据此写出反应的化学方程式;
(4)根据探究二氧化碳的性质既不能燃烧也不支持燃烧且密度比空气大的实验来分析;
(5)学会检验二氧化碳气体的方法及其化学方程式的书写;
(6)根据装置特点来选择制取氧气的药品去分析解答;
(7)根据收集气体的方法以及气体的性质来分析;
(8)根据已有的知识进行分析,酸性溶液能使紫色石蕊试液变成红色,水和二氧化碳不能使紫色石蕊试液变色.
解答 解:(1)检查A装置的气密性的方法是:在右导管口连一乳胶管,在乳胶管 上夹弹簧夹,向长颈漏斗内加水,至形成液封,再加适量水,静置一段时间后,若长颈漏斗液面与试管内液面差保持不变,说明气密性良好;故填:在右导管口连一乳胶管,在乳胶管 上夹弹簧夹,向长颈漏斗内加水,至形成液封,再加适量水,静置一段时间后,若长颈漏斗液面与试管内液面差保持不变,说明气密性良好;
(2)装置改进后的有孔板可以把固体与液体分离开来,当关闭导管时,装置内压强升高而把液体压回长颈漏斗,使得液体与固体脱离接触反应停止,当打开导管,装置内压强减小,长颈漏斗内液体重新流入装置,液体与固体接触,反应继续;故填:随开随制,随关随停;
(3)大理石的主要成分是碳酸钙,碳酸钙和稀盐酸反应生成了氯化钙、水和二氧化碳,其反应的化学方程式为:CaCO3+2HCl═CaCl2+H2O+CO2↑.故填:CaCO3+2HCl=CaCl2+CO2↑+H2O;
(4)将D中的CO2倒入C中做性质实验时,操作方法是沿烧杯壁慢慢倒入,避免迅速倒入时,蜡烛熄灭的先后次序不明显,导致实验失败;正确的观察现象是蜡烛火焰由低到高依次熄灭,体现了二氧化碳既不能燃烧也不支持燃烧且密度比空气大的性质.故答案为:将二氧化碳沿烧杯壁慢慢倒入;蜡烛由低到高依次熄灭;不能燃烧也不支持燃烧;密度比空气大.
(5)检验二氧化碳气体的方法:将制得的二氧化碳气体通入盛有澄清石灰水的试管中,观察到的现象是:澄清石灰水变浑浊;其反应的化学方程式为:CO2+Ca(OH)2=CaCO3↓+H2O.故填:CO2+Ca(OH)2=CaCO3↓+H2O;
(6)图中装置适合用于过氧化氢溶液在二氧化锰催化作用下生成水和氧气;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(7)难溶于水,不与水反应的气体用排水法进行收集;一氧化碳的密度比水小,所以用F收集一氧化碳时,气体从短管进入;故填:难溶于水且不和水反应;b;
(8)①稀盐酸是酸性溶液,能使石蕊试液变红,水和二氧化碳不能使石蕊试液变色,二氧化碳的水溶液能使石蕊试液变红,故填:纸花不变色;纸花变红;
②盐酸使紫色石蕊试液变红;水不能使紫色石蕊试液变红,故填:使纸花变红是酸不是水;
③进行对比实验说明二氧化碳本身不显酸性,不能使石蕊变色,二氧化碳的水溶液显酸性,能使石蕊变红,故填:二氧化碳不能使石蕊变色,二氧化碳的水溶液能使石蕊变红;
④二氧化碳能与水反应生成碳酸,故填:CO2+H2O═H2CO3.
点评 此题探究了实验室制取二氧化碳气体的装置及改进后的优点,考查了二氧化碳气体的检验方法并会写其反应的化学方程式;还探究了二氧化碳既不能燃烧也不支持燃烧且密度比空气大的性质的实验.题型设计科学,是常考题型之一.

 阅读快车系列答案
阅读快车系列答案| A. | 空气与氧气--带火星的木条 | B. | 空气和二氧化碳--澄清石灰水 | ||
| C. | 二氧化碳和氮气--石灰水 | D. | 氮气与二氧化碳--燃着的木条 |
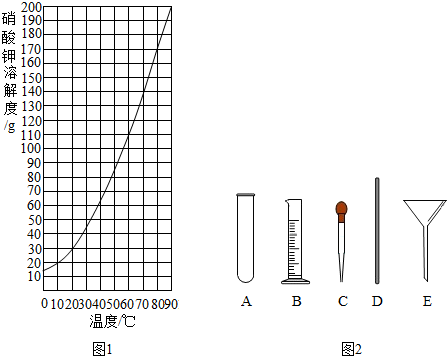
(1)查阅硝酸钾溶解性.由图可知,20℃时,硝酸钾的溶解度为31.6g,在该温度下配制硝酸钾溶液,溶质质量分数最大为24%(计算结果保留整数).
(2)计算.配制40g质量分数为10%的硝酸钾溶液,所需硝酸钾的质量为4g,所需蒸馏水的体积为36mL
(3)称量.分别在天平左右两盘放上纸片,调节平衡后,A(填字母).
A.先移动游码到所需位置,再添加硝酸钾直到天平平衡
B.先添加所需的硝酸钾,再移动游码直到天平平衡
(4)量取.量取所需蒸馏水要用到的仪器是图2中的BC(填字母).
(5)溶解.将称量好的硝酸钾和蒸馏水混合溶解.
(6)稀释.20℃时,将20mL质量分数为10%的硝酸钾溶液,稀释成质量分数为4%的硝酸钾溶液.从表中找出需要用到的数据:g/mL.
硝酸钾溶液的密度(单位g/mL)
| 温度/℃ 质量分数/% | 20 | 40 | 60 |
| 4 | 1.023 | 1.016 | 1.007 |
| 10 | 1.063 | 1.054 | 1.044 |
【实验】用天平称量0.2gCuO,取5mL5%的过氧化氢溶液于试管中,进行如图实验:

(1)填写如表:
| 步骤③现象 | 步骤⑥结果 | 步骤⑦现象 | 结论 |
| 溶液中产生气泡较快 带火星的木条复燃. | 固体质量不变 | 溶液中有气泡放出, 带火星的木条复燃 | 猜想成立. |
(3)步骤④需用到的实验仪器有:铁架台(带铁圈)、漏斗、烧杯、玻璃棒.
(4)过氧化氢能被CuO催化分解放出O2的化学方程式为2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
(5)请你帮助小芳同学设计实验证明步骤⑤所得固体确实已经烘干,你的方案为:在固体上加无水硫酸铜,固体不变蓝,说明已经烘干.