题目内容
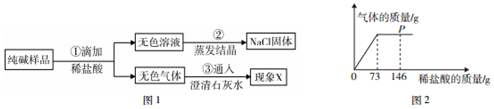
16.小明在协助老师清理实验室储备室时,发现一瓶存放多年的氢氧化钙.为检验其变质情况,进行如 下探究:取氢氧化钙样品11.4g于锥形瓶中,加入38.6g水,然后逐渐滴加14.6%的稀盐酸,加入稀盐酸的质量与锥形瓶中物质的质量关系如图1所示.请问: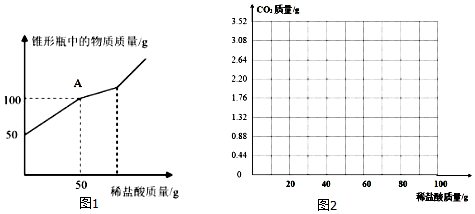
(1)与氢氧化钙反应的稀盐酸的质量为50g.
(2)A点时所得溶液的溶质质量分数(结果精确到0.1%).
(3)根据计算所得数据在图2中画出生成CO2的质量的曲线,并进行必要的标注.
分析 本题计算建立在样品只含氢氧化钙和碳酸钙的前提下,而不含水等杂质.
(1)样品加水共50g,加入50g稀盐酸时物质总质量为100g,此时无气体生成,说明只是和氢氧化钙反应.可判断与氢氧化钙反应的稀盐酸的质量;
(2)A点时是氢氧化钙和稀盐酸恰好完全反应,而此时碳酸钙没有参与反应,所以得到的溶液的溶质只有氯化钙,且是氢氧化钙和50g14.6%的稀盐酸反应所得,进而根据对应的化学方程式求算氯化钙的质量,进而求算对应的质量分数.
(3)根据碳酸钙的质量和对应的化学方程式求算消耗的稀盐酸的质量和生成的二氧化碳的质量,进而描绘出对应的曲线图.
解答 解:本题计算建立在样品只含氢氧化钙和碳酸钙的前提下,而不含水等杂质.
样品加水共50g,加入50g稀盐酸时物质总质量为100g,此时无气体生成,说明只是和氢氧化钙反应.可判断与氢氧化钙反应的稀盐酸的质量为50g;此时得到的溶液中溶质为氢氧化钙和50g14.6%的稀盐酸反应得到的氯化钙.
设生成的氯化钙的质量为x,消耗的氢氧化钙的质量为y
Ca(OH)2+2HCl=CaCl2+2H2O
74 73 111
y 50g×14.6% x
$\frac{74}{y}$=$\frac{73}{50g×14.6%}$=$\frac{111}{x}$
x=11.1g
y=7.4g
样品中碳酸钙的质量为11.4g-7.4g=4g
A点所得溶液的溶质质量分数为$\frac{11.1g}{100g-4g}$×100%≈11.6%
设4g碳酸钙反应消耗的稀盐酸的质量为z,生成的二氧化碳的质量为a
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 73 44
4g 14.6%z a
$\frac{100}{4g}$=$\frac{73}{14.6%z}$=$\frac{44}{a}$
z=20g
a=1.76g
即加入盐酸到70g时生成1.76g的二氧化碳,得图.
故答案为:
(1)与氢氧化钙反应的稀盐酸的质量为 50g.
(2)A点时所得溶液的溶质质量分数为11.6%.
(3)
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

| A. | 生石灰 | B. | 纯碱 | C. | 氯化氢 | D. | 食盐 |
| A. |  白磷 | B. |  氢气 | C. |  氢氧化钠 | D. |  浓硫酸 |
| A. | 酒精--洗去手上的油污 | |
| B. | 食醋--除去保温瓶胆内壁的水垢 | |
| C. | 食盐水--除去衣服上的锈溃 | |
| D. | 纯碱--除去沾附在鱼肉上的鱼胆汁(显酸性)的苦味 |
| A. |  黄铜片能在铜片上刻画出痕迹可以说明黄铜的硬度比铜片大 | |
| B. |  无色酚酞试液变红既可以说明分子在不停的运动着,又可以说明氨水显碱性 | |
| C. |  既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 | |
| D. | 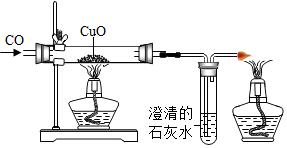 既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
 小明利用电解水的简易装置探究水的组成.通电一段时间后,现象如图所示,则试管a收集到的气体是氢气,与该试管相连的是电源的负极;试管b中的气体可以用带火星的木条来检验.通过该实验得出的结论是水是由氢元素和氧元素组成,该变化过程中是将电转化为化学能.进行该试验时往往会在水中加入稀硫酸或氢氧化钠,其目的是增强水的导电性.
小明利用电解水的简易装置探究水的组成.通电一段时间后,现象如图所示,则试管a收集到的气体是氢气,与该试管相连的是电源的负极;试管b中的气体可以用带火星的木条来检验.通过该实验得出的结论是水是由氢元素和氧元素组成,该变化过程中是将电转化为化学能.进行该试验时往往会在水中加入稀硫酸或氢氧化钠,其目的是增强水的导电性.