题目内容
某化学兴趣小组在甲、乙两个充满O2的密闭容器中各加入一定量的碳粉,在高温条件下使其充分反应,待反应结束后,两个容器中的碳粉都已完全消失.该小组成员对两容器中反应后的气体进行如下探究:
(1)小红同学对甲容器中气体的组成提出如下四种猜想:
①只有CO ②只有CO2 ③只有O2 ④CO和O2的混合气体
你认为上述猜想中明显不合理的有 (填序号).
(2)小明同学认为甲容器中的气体还可能是CO和CO2的混合气体,为了验证自己的猜想,他准备按如图所示装置进行探究.
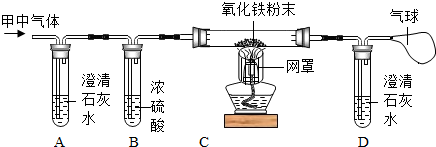
请你回答下列问题:
①装置B中浓硫酸的作用是 .
②若小明的猜想成立,则装置A中的实验现象是 ,反应的化学方程式 .装置C玻璃管中的实验现象是 ,反应的化学方程式是 .
(3)小芳同学对乙容器中气体的组成提出了除上述猜想外的另一种合理猜想,她的猜想是 ,于是她设计了下列实验方案验证其猜想:
【步骤1】先加热装有铜丝网的玻璃管一段时间后,再通入乙中的气体,观察现象.
【步骤2】将乙中的气体通入澄清石灰水中,观察现象.
指导老师在分析其实验方案后,指出了其中存在的错误或不足.
①步骤1应先通入乙中气体一段时间后方可加热,你认为这样修改的原因是 .
②没有必要进行步骤2的实验,其理由是 .
(4)若反应前甲、乙两容器中炭粉与氧气的质量比分别表示为(
)甲和(
)乙,当小明和小芳的猜想均成立时,则 (
)甲 (
)乙填“>”“<”或“=”).
(1)小红同学对甲容器中气体的组成提出如下四种猜想:
①只有CO ②只有CO2 ③只有O2 ④CO和O2的混合气体
你认为上述猜想中明显不合理的有
(2)小明同学认为甲容器中的气体还可能是CO和CO2的混合气体,为了验证自己的猜想,他准备按如图所示装置进行探究.

请你回答下列问题:
①装置B中浓硫酸的作用是
②若小明的猜想成立,则装置A中的实验现象是
(3)小芳同学对乙容器中气体的组成提出了除上述猜想外的另一种合理猜想,她的猜想是
【步骤1】先加热装有铜丝网的玻璃管一段时间后,再通入乙中的气体,观察现象.
【步骤2】将乙中的气体通入澄清石灰水中,观察现象.
指导老师在分析其实验方案后,指出了其中存在的错误或不足.
①步骤1应先通入乙中气体一段时间后方可加热,你认为这样修改的原因是
②没有必要进行步骤2的实验,其理由是
(4)若反应前甲、乙两容器中炭粉与氧气的质量比分别表示为(
| m c |
| m o 2 |
| m c |
| m o 2 |
| m c |
| m o 2 |
| m c |
| m o 2 |
考点:实验探究物质的组成成分以及含量,常见气体的检验与除杂方法,一氧化碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)碳在氧气中充分燃烧是二氧化碳,不充分燃烧生成一氧化碳;
(2)二氧化碳能使澄清石灰水变浑浊,一氧化碳能还原氧化铁,根据反应物和生成物,按照书写化学方程式的步骤完成化学方程式;
(3)从氧气过量的角度考虑生成物,灼热的铜能和氧气反应生成氧化铜;
(4)氧气的质量一定,根据碳的多少判断比值的大小.
(2)二氧化碳能使澄清石灰水变浑浊,一氧化碳能还原氧化铁,根据反应物和生成物,按照书写化学方程式的步骤完成化学方程式;
(3)从氧气过量的角度考虑生成物,灼热的铜能和氧气反应生成氧化铜;
(4)氧气的质量一定,根据碳的多少判断比值的大小.
解答:解:(1)因为碳在氧气中充分燃烧是二氧化碳,不充分燃烧生成一氧化碳;故生成物有可能是二氧化碳,一氧化碳,或二氧化碳和一氧化碳的混合物,或二氧化碳和氧气的混合物;不可能只有氧气,因为有碳参加了反应,也不能是一氧化碳和氧气混合物,如果剩余这两种气体它们会继续反应;故选③④;
(2)验证一氧化碳和二氧化碳的混合气体时,要先用石灰水检验二氧化碳,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;再用氧化铁和石灰水检验一氧化碳,化学方程式为:3CO+Fe2O3
2Fe+3CO2;
(3)当氧气过量时,乙容器中的混合气体是氧气和二氧化碳的混合物,验证这种组合时主要是检验氧气的存在,检验氧气可通过灼热的网,注意开始反应时要把装置内的空气排出,防止空气中的氧气对实验结果造成影响;
(4)氧气的质量一定,甲容器中生成一氧化碳,说明氧气量不足,说明碳多,乙容器内氧气有剩余,说明碳少,故(
)甲>(
)乙.
故答案为:
(1)③④;
(2)①干燥气体; ②澄清石灰水变浑浊; CO2+Ca(OH)2═CaCO3↓+H2O;
红色粉末变为黑色; 3CO+Fe2O3
2Fe+3CO2;
(3)氧气和二氧化碳; ①排净玻璃管中的空气,排除空气中氧气的干扰; ②碳在充足的氧气中燃烧生成二氧化碳;
(4)>
(2)验证一氧化碳和二氧化碳的混合气体时,要先用石灰水检验二氧化碳,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;再用氧化铁和石灰水检验一氧化碳,化学方程式为:3CO+Fe2O3
| ||
(3)当氧气过量时,乙容器中的混合气体是氧气和二氧化碳的混合物,验证这种组合时主要是检验氧气的存在,检验氧气可通过灼热的网,注意开始反应时要把装置内的空气排出,防止空气中的氧气对实验结果造成影响;
(4)氧气的质量一定,甲容器中生成一氧化碳,说明氧气量不足,说明碳多,乙容器内氧气有剩余,说明碳少,故(
| m c |
| m o 2 |
| m c |
| m o 2 |
故答案为:
(1)③④;
(2)①干燥气体; ②澄清石灰水变浑浊; CO2+Ca(OH)2═CaCO3↓+H2O;
红色粉末变为黑色; 3CO+Fe2O3
| ||
(3)氧气和二氧化碳; ①排净玻璃管中的空气,排除空气中氧气的干扰; ②碳在充足的氧气中燃烧生成二氧化碳;
(4)>
点评:此题是对碳与氧气反应的知识的考查,解决的关键是对可能组合问题的探讨,然后根据不同组合的物质的性质进行实验验证,此题难度较大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
如图是水分子电解模型,由此模型所获得的信息中,不正确的是( )
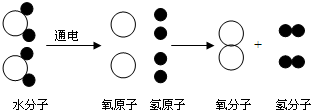

| A、水是由氢和氧两种元素组成 |
| B、反应物的原子总数等于生成物的原子总数 |
| C、一个水分子由两个氢原子和一个氧原子构成 |
| D、一个水分子由两个氢分子和一个氧原子构成 |
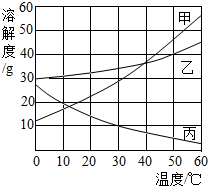 甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:
甲、乙、丙三种物质的溶解度曲线如图所示.据图回答:(1)50℃时,乙物质的溶解度是
(2)30℃时,三种物质的溶解度由大到小的顺序为
(3)要使接近饱和的丙物质变为饱和,可以采取的一种措施是
用托盘天平称量6.8g食盐,若指针偏向右边,则应( )
| A、在左盘增加称物量 |
| B、移动游码使天平平衡 |
| C、减少左盘上的食盐 |
| D、增加砝码使天平平衡 |
表中列出了几种物质的熔点,据此判断下列说法正确的是( )
| 物质名称 | 汞 | 金 | 铜 | 铁 | 钨 | 氧 |
| 熔点(℃) | -38.8 | 1064 | 1083 | 1535 | 3410 | -218 |
| A、液氧在常温下保存必须加高压 |
| B、水银温度计可测量-40℃的温度 |
| C、“真金不怕火炼”说明金的熔点最高 |
| D、用钨制灯丝是因为其在高温下也不易氧化 |
下列实验操作,错误的是( )
A、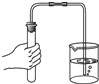 检查装置的气密性 |
B、 读取水的体积 |
C、 点燃酒精灯 |
D、 倾倒液体 |
 如图,用红磷燃烧来测定空气中氧气的含量,发生的实验现象是:
如图,用红磷燃烧来测定空气中氧气的含量,发生的实验现象是: