题目内容
13.现有一包粉末,已知他们可能是由Na2SO4 CuCl2 Na2CO3 KNO3 中的一种或几种组成,某同学的实验记录如下:
A的化学式为BaCO3,D的化学式为CO2
由上述推断,原粉末中一定不含CuCl2、Na2SO4
无色溶液B中一定含有的溶质是NaCl,可能含有的溶质是KNO3
写出生成白色沉淀A的化学方程式BaCl2+Na2CO3═BaCO3↓+2NaCl生成无色气体D的化学方程式BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑.
分析 如果溶液无色,则证明溶液中不含铜离子,可排除CuCl2;白色沉淀可溶于稀硝酸,说明此白色沉淀不是BaSO4,排除Na2SO4;白色沉淀溶于稀硝酸,说明此白色沉淀为BaCO3,故一定有Na2CO3;然后根据反应现象,确定其它物质.
解答 解:1、因为第一次反应生成白色沉淀和无色溶液,故可判断肯定没有CuCl2,因为有铜离子的溶液都是蓝色或蓝绿色;
2、加适量氯化钡溶液,生成白色沉淀A且沉淀可溶于稀硝酸,说明此白色沉淀A为BaCO3沉淀而不是BaSO4;又因为在所给的四种物质中,只有Na2CO3含有碳酸跟离子,故可判定粉末中一定有Na2CO3,一定没有Na2SO4;故无色溶液B中的溶质为NaCl,可能有KNO3;
3、由2的分析可知,白色沉淀A为碳酸钡,与稀硝酸反应,生成硝酸钡、水和二氧化碳气体,故可判断无色溶液C为硝酸钡溶液,无色气体D为CO2.
故答案为:BaCO3;CO2; CuCl2,Na2SO4; NaCl;KNO3;BaCl2+Na2CO3═BaCO3↓+2NaCl;BaCO3+2HNO3═Ba(NO3)2+H2O+CO2↑.
点评 此题主要是考查学生的综合分析能力,不但要求学生具备有关化合物的基础知识,而且要有实验操作的经历和分析、解决化学实验问题的能力.解题时需要认真分析题目给出的条件,联系实际,逐一分析推断.

练习册系列答案
相关题目
3.下列关于分子、原子、离子构成物质的说法中,不正确的是( )
| A. | 汞原子聚集成金属汞 | |
| B. | 氮原子结合成氮气 | |
| C. | 氧原子和氢原子结合成水分子,水分子聚集成水 | |
| D. | 氯原子和钠原子得失电子形成氯离子和钠离子,两种离子结合成氯化钠 |
1.下图所示的实验中,发生了化学变化的是( )
| A. |  干冰升华 | B. |  CO2溶于水 | ||
| C. | 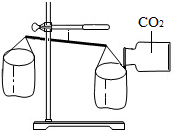 实验CO2的密度 | D. |  自制过滤器过滤液体 |
8.下列过程中,属于物理变化的是( )
| A. |  测定溶液pH | B. |  樟脑球变小 | ||
| C. |  点燃的钠放入氯气中 | D. |  浓硫酸使蔗糖变黑 |
1.我们生活在物质世界里,下列叙述中不涉及化学变化的是( )
| A. | 不纯的氢气燃烧发生爆炸 | B. | 涂在墙上的熟石灰逐渐变硬 | ||
| C. | 焦炭冶炼金属 | D. | 舞台上用干冰制造“云雾” |
 e.
e.

 如图是电解水的简易装置.
如图是电解水的简易装置.