题目内容
根据图1、图2回答问题:
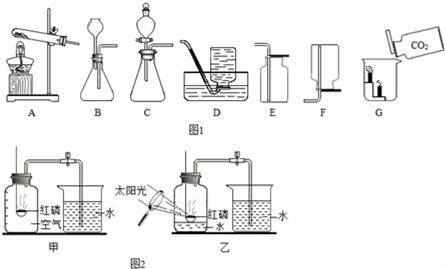

(1)写出A中用于支持的仪器的名称 .
(2)实验室利用氯酸钾和二氧化锰制取氧气,选用的发生装置是 (填序号).其化学方程式为 .收集较纯净的氧气,应选用的装置是 (填序号).
(3)实验室制取CO2的化学方程式为 .装置B和C都可以用来制取CO2,其中装置C的优点在于 .某同学收集CO2气体,应选用的装置是 (填序号),将这瓶气体按图G所示倒入烧杯中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质是 CO .
(4)图2中甲中冷却至室温时,打开止水夹可观察到 现象.科学贵在创新,图2中乙是对甲测定空气中氧气含量的实验的改进(甲中红磷用酒精灯点燃),你认为改进后的优点 .
【考点】二氧化碳的实验室制法;空气组成的测定;氧气的制取装置;氧气的收集方法;二氧化碳的物理性质;二氧化碳的化学性质;书写化学方程式、文字表达式、电离方程式.
【分析】(1)根据实验室常用仪器解答;
(2)利用二氧化锰作催化剂加热氯酸钾制氧气是固体加热,选取发生装置;因为氧气密度比空气大,且不易溶于水解答.
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;
(4)图2乙装置设计的比较好,操作简单,并且试管内的空气也不会逸出来,比较严密.
【解答】解:
(1)根据实验室常用仪器可知:A中用于支持的仪器的名称铁架台;
(2)利用二氧化锰作催化剂加热氯酸钾制氧气是固体加热,因此选取发生装置为A;因为氧气密度比空气大,且不易溶于水,所以收集装置可以是:DE;若收集较纯净的氧气,应选择的收集装置是D,用二氧化锰作催化剂加热氯酸钾制氧气,反应的化学方程式为:2KClO3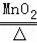
 2KCl+3O2↑;
2KCl+3O2↑;
(3)实验室制取CO2,是在常温下,用碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,其化学方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;装置B和C都可以用来制取CO2,其中装置C的优点在于控制反应速率.某同学收集CO2气体,应选用的装置是E,将这瓶气体按图G所示倒入烧杯中,观察到蜡烛自下而上依次熄灭,说明二氧化碳具有的物理性质是CO2密度比空气大.
(4)图2中甲中冷却至室温时,打开止水夹可观察到集气瓶内水位上升至
 处现象.用酒精灯引燃红磷,红磷燃烧生成了五氧化二磷进入空气会污染空气,由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出.科学贵在创新,图2中乙通过凸透镜聚光引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确,故误差少或减少污染.所以实验改进后的优点在密封的容器中进行,防止P2O5污染空气.
处现象.用酒精灯引燃红磷,红磷燃烧生成了五氧化二磷进入空气会污染空气,由于磷燃烧放出大量的热,打开瓶塞时容易使空气受热而逸出.科学贵在创新,图2中乙通过凸透镜聚光引燃红磷,不需要打开瓶塞,空气出不来也进不去,测量比较准确,故误差少或减少污染.所以实验改进后的优点在密封的容器中进行,防止P2O5污染空气.
故答案为:
(1)铁架台;(2)A,2KC1O3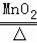
 2KC1+3O2↑,D;
2KC1+3O2↑,D;
(3)CaCO3+2HCl=CaCl2+H2O+CO2↑;控制反应速率;E,CO2密度比空气大;
(4)集气瓶内水位上升至
 处;在密封的容器中进行,防止P2O5污染空气.
处;在密封的容器中进行,防止P2O5污染空气.

 轻松课堂单元期中期末专题冲刺100分系列答案
轻松课堂单元期中期末专题冲刺100分系列答案一定条件下,下列物质在密闭容器内充分反应,测得反应前后各物质的质量如下:
| 物质 | A | B | C | D |
| 反应前的质量/g | 1.7 | 2.2 | 7.9 | 0.9 |
| 反应后的质量/g | 待测 | 6.6 | 0 | 2.7 |
则反应后A的质量为 ;该反应所属的基本反应类型是 ;该反应中B和D两种物质变化的质量比为 .
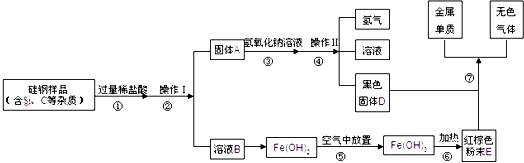
 氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).
氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO2+2H2↑).