题目内容
17.金属在生产生活中应用广泛.(1)铝可以制成铝箔,这是利用金属铝具有良好的延展性.
(2)铁制品生锈的条件是与氧气、水接触,用稀盐酸除铁锈反应的化学方程式是Fe2O3+6HCl=2FeCl3+3H2O
(3)工业上冶炼铝,是将铝矿石(主要成分是Al2O3)在熔融条件下通电分解,其反应的化学方程式是2Al2O3$\frac{\underline{\;通电\;}}{熔融}$4Al+3O2↑.
分析 (1)根据物质的性质决定其用途分析;
(2)根据铁生锈的条件和用稀盐酸除锈的原理进行分析;
(3)根据反应原理结合化学方程式的书写分析.
解答 解:(1)金属铝具有良好的延展性,因此铝可以制成铝箔;
(2)铁制品生锈的条件是与潮湿的空气接触;铁锈的主要成分是氧化铁,稀盐酸和氧化铁反应生成氯化铁和水,因此用稀盐酸除铁锈反应的化学方程式是Fe2O3+6HCl=2FeCl3+3H2O;
(3)铝矿石(主要成分是Al2O3)在熔融条件下通电分解生成铝和氧气,其反应的化学方程式是2Al2O3$\frac{\underline{\;通电\;}}{熔融}$4Al+3O2↑;
故答案为:
(1)延展;(2)与氧气、水接触;Fe2O3+6HCl=2FeCl3+3H2O;(3)2Al2O3$\frac{\underline{\;通电\;}}{熔融}$4Al+3O2↑.
点评 本题体现了化学与生活的紧密联系,加强金属的知识的学习,解决好有关金属在生产生活中应用广泛的一些问题.

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
7.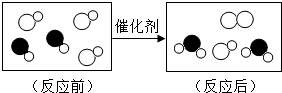 “尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,下面是其中一个化学反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )
“尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,下面是其中一个化学反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )
 “尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,下面是其中一个化学反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )
“尾气催化转化器”可以将汽车尾气中有毒气体转变为无毒气体,下面是其中一个化学反应的微观示意图,其中不同的圆球代表不同的原子.从图中获得信息不正确的是( )| A. | 化学反应的实质是生成了新分子 | |
| B. | 分子间存在着一定的空隙 | |
| C. | 图中生成物均为化合物 | |
| D. | 参加反应的两种分子的个数比为1:1 |
5.下列从如图中获得的信息不正确的是( )


| A. | 该元素在地壳中的含量为为28.09% | B. | 该元素符号为Si | ||
| C. | 由该元素组成的单质常温下为固体 | D. | 该元素属于非金属元素 |
2.梧州市的“六堡茶”畅销全国各地,“茶香阵阵”这是因为( )
| A. | 分子在不断运动 | B. | 分子质量很小 | C. | 分子间有间隔 | D. | 分子可以再分 |
9.下列燃料的使用对环境的污染程度最小的是( )
| A. | 煤 | B. | 天然气 | C. | 氢气 | D. | 汽油 |
12.2008年,我市被确认为浙江省卫生城市,下列不利于“创建卫生城市”的行为是( )
| A. | 按规定停放车辆 | B. | 不随意丢弃废电池 | ||
| C. | 回收使用过的塑料、橡胶 | D. | 在绿化带堆放杂物 |
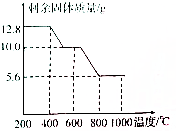 草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解:CaC2O4$\frac{\underline{\;400~500℃\;}}{\;}$CaCO3+CO↑.为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量与温度的关系如图所示.
草酸钙(CaC2O4)是一种难溶于水的白色固体,受热能分解:CaC2O4$\frac{\underline{\;400~500℃\;}}{\;}$CaCO3+CO↑.为了探究其在加热条件下发生的变化,进行如下实验:取12.8g草酸钙固体在不断加热的条件下测得剩余固体的质量与温度的关系如图所示.